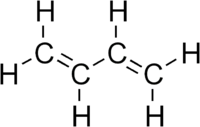
Butadieno
| ||||||||||||||||||||
Butadieno. Alqueno producido en la destilación del petróleo, se conoce además como 1,3-butadieno. Es un gas incoloro de olor levemente parecido a la gasolina.
Sumario
Reseña histórica
El Butadieno fue aislado en 1863, como un hidrocarburo desconocido mediante la pirólisis del Alcohol amílico. Y luego en 1886, se identificó como butadieno por Henry Edward Armstrong, el cual lo aisló a través de los productos de pirólisis del petróleo.
En 1910, el químico ruso Sergei Lebedev obtuvo el butadieno polimerizado, con propiedades similares al caucho. Este polímero es, sin embargo, demasiado suave para sustituir el caucho natural en muchas funciones, sobre todo los neumáticos del automóvil.
La industria de butadieno se originó en los años previos a la Segunda Guerra Mundial. Muchas de las naciones beligerantes se dieron cuenta de que, en caso de guerra, podrían ser separados de las plantaciones de caucho controlado por el Imperio Británico, y trataron de eliminar su dependencia del caucho natural.
En 1929, Eduard Tschunker y Bock Walter, trabajando para IG Farben en Alemania, hizo un copolímero de estireno y butadieno, que podría ser utilizado en los neumáticos del automóvil. La producción mundial se disparó rápidamente, con butadieno que se produce a partir de alcohol de grano en la antigua Unión Soviética y los Estados Unidos y de acetileno derivado del carbón en Alemania.
Propiedades
El nombre Butadieno también puede hacer referencia a su isómero, 1,2-butadieno. Aunque su importancia es casi nula al lado del 1,3-butadieno.
Cerca del 75% del 1,3-butadieno que se manufactura se usa para fabricar caucho sintético. El caucho sintético es usado extensamente en neumáticos para automóviles y camiones. También se usa para fabricar plásticos, entre los que se incluyen los acrílicos. La gasolina contiene pequeñas cantidades de 1,3-butadieno.
Aplicaciones
La mayoría del butadieno se polimeriza para producir caucho sintético. Mientras que el polibutadieno es en sí muy suave, casi líquido, los copolímeros preparados a partir de mezclas de butadieno con estireno y/o de acrilonitrilo, tales como acrilonitrilo butadieno estireno (ABS), acrilonitrilo-butadieno (NBR) y estireno-butadieno (SBR) son resistentes y elásticos .
El butadieno se utiliza en la producción industrial de 4-vinilciclohexeno a través de una reacción de dimerización de Diels Alder. El vinilciclohexeno es una impureza común que se encuentra en el almacenamiento de butadieno. El Ciclooctadieno y el ciclododecatrieno se producen a través de reacciones dimerizadas y trimerizadas, catalizadas por níquel y titanio, respectivamente.
El Butadieno también es útil en la síntesis de cicloalcanos y cicloalquenos, ya que reacciona con los dobles y los triples enlaces través de la reacción de Diels-Alder.
Interacción con el medio ambiente
¿Qué le sucede al 1,3-butadieno cuando entra al Medio Ambiente?
- Se evapora rápidamente al aire como gas a causa de escapes durante la producción, uso, almacenamiento, transporte o disposición.
- En el aire, la luz solar lo degrada rápidamente; en días de sol, la mitad del 1,3-butadieno en el aire se degrada en aproximadamente 2 horas.
- En ausencia de luz solar, la mitad del 1,3-butadieno en el aire se degrada en unos pocos días.
- Se evapora rápidamente desde el agua y el suelo.
- Como se evapora tan fácilmente, es improbable que se encuentre en el agua o en el suelo. No existen métodos adecuados para medir las cantidades de 1,3-butadieno en agua o suelo.
- En el suelo puede ser degradado por microorganismos.
- No se acumula en peces.
Fuentes
- Morrison, R. T. y Boyd, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, Estados Unidos, 1990.
- Soto, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996.
- Monografías.com
- Química Orgánica
- Butadieno