Diferencia entre revisiones de «Guanidina»
(Página creada con ' {{Definición |nombre= Guanidina |imagen= Guanidina.png |tamaño= |concepto= Es una Sustancia blanca e higroscópica. Se encuentra de manera...') |
(→Fuentes) (Etiqueta: revisar proyecto) |
||
| (No se muestra una edición intermedia de otro usuario) | |||
| Línea 8: | Línea 8: | ||
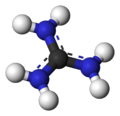
'''Guanidina''' es el único derivado trifuncional importante del [[Ácido carbónico]], fue descubierta como un producto de descomposición de la [[Guanina]], su formula molecular es CH5N3 | '''Guanidina''' es el único derivado trifuncional importante del [[Ácido carbónico]], fue descubierta como un producto de descomposición de la [[Guanina]], su formula molecular es CH5N3 | ||
== Propiedades físicas == | == Propiedades físicas == | ||
| − | La guanidina es un compuesto puro de color blanco, cristalino y muy alcalino, con una temperatura de fusión de 323,15 K (50 °C) | + | La guanidina es un compuesto puro de color blanco, cristalino y muy alcalino, con una temperatura de fusión de 323,15 K (50 °C)y una masa molecular de 59,07 g/mol, |
== Preparación == | == Preparación == | ||
| − | Se forma a partir de la oxidación de la guanina y | + | Se forma a partir de la oxidación de la guanina y la podemos encontrar de manera natural en la orina como un producto normal del metabolismo de las proteínas. |
== Propiedades químicas == | == Propiedades químicas == | ||
Su acumulación en el cuerpo, como en casos de enfermedad renal de crónica, está asociada con neurotoxicidad. | Su acumulación en el cuerpo, como en casos de enfermedad renal de crónica, está asociada con neurotoxicidad. | ||
Es una base monoácida fuerte, sus soluciones absorben [[Dióxido de carbono]] del [[aire]] dando Carbonato de guanidina. | Es una base monoácida fuerte, sus soluciones absorben [[Dióxido de carbono]] del [[aire]] dando Carbonato de guanidina. | ||
| − | La presencia de tres grupos aminos en la guanidina puede hacer suponer de que será tribásica. Sin embargo la aceptación de un [[Protón]] da un ión guanidinio en el que la carga positiva es igualmente compartida por todos los [[Átomos]] de [[ | + | La presencia de tres grupos aminos en la guanidina puede hacer suponer de que será tribásica. Sin embargo la aceptación de un [[Protón]] da un [[ión]] guanidinio en el que la carga positiva es igualmente compartida por todos los [[Átomos]] de [[Nitrógeno]] |
== Aplicaciones == | == Aplicaciones == | ||
Se usa en la fabricación de [[Plásticos]], [[Cauchos]] y [[Explosivos]]. No se debe confundir con la [[Guanina]], una de las bases que forman el [[ADN]], ni con la [[Guanosina]], su nucleósido. | Se usa en la fabricación de [[Plásticos]], [[Cauchos]] y [[Explosivos]]. No se debe confundir con la [[Guanina]], una de las bases que forman el [[ADN]], ni con la [[Guanosina]], su nucleósido. | ||
| Línea 24: | Línea 24: | ||
* http://es.wikipedia.org/wiki/Guanidina | * http://es.wikipedia.org/wiki/Guanidina | ||
| − | [[ | + | [[Categoría: Ácidos nucleicos]] |
| + | [[Categoría: Moléculas orgánicas]] | ||
última versión al 12:24 19 oct 2018
| ||||||
Guanidina es el único derivado trifuncional importante del Ácido carbónico, fue descubierta como un producto de descomposición de la Guanina, su formula molecular es CH5N3
Propiedades físicas
La guanidina es un compuesto puro de color blanco, cristalino y muy alcalino, con una temperatura de fusión de 323,15 K (50 °C)y una masa molecular de 59,07 g/mol,
Preparación
Se forma a partir de la oxidación de la guanina y la podemos encontrar de manera natural en la orina como un producto normal del metabolismo de las proteínas.
Propiedades químicas
Su acumulación en el cuerpo, como en casos de enfermedad renal de crónica, está asociada con neurotoxicidad. Es una base monoácida fuerte, sus soluciones absorben Dióxido de carbono del aire dando Carbonato de guanidina. La presencia de tres grupos aminos en la guanidina puede hacer suponer de que será tribásica. Sin embargo la aceptación de un Protón da un ión guanidinio en el que la carga positiva es igualmente compartida por todos los Átomos de Nitrógeno
Aplicaciones
Se usa en la fabricación de Plásticos, Cauchos y Explosivos. No se debe confundir con la Guanina, una de las bases que forman el ADN, ni con la Guanosina, su nucleósido. Actualmente se está analizando la posibilidad de utilizar la guanidina como un Combustible alternativo. En presencia de un Catalizador, un mol de guanidina se combina con 2 moles de Agua para dar 3 moles de Amoníaco y 1 mol de Dióxido de carbono.
Fuentes
- Brewster, Ray Q. Mcewen, Willian E. Química Orgánica/ Ray Q Brewster, Willian E Mcewen Instituto Cubano del Libro. La Habana. Edición Revolucionaria. 1975_950p.