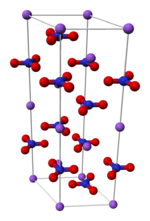
Nitrato de sodio
| ||||||||||||||
Nitrato de Sodio. nitrato sódico, sal de Chile o nitrato de Chile cuya fórmula química es NaNO3 es un agente preventivo de la enfermedad conocida como .botulismo También es conocido como salitre.
Sumario
Sintésis
El nitrato de sodio se obtiene por neutralización de bases de carbono(e.g. hidróxido sódico = NaOH o carbonato sódico = Na2CO3) con ácido nítrico HNO3. Es un subproducto en la síntesis del ácido nítrico donde se forma al absorber el dióxido de nitrógeno en una disolución de carbonato sódico: Na2CO3 + 2 NO2 -> NaNO3 + NaNO2 + CO2 Además existen yacimientos importantes naturales de esta sal en Chile de donde recibe también la denominación de "Sal de Chile" o "Nitrato de Chile".
Propiedades
Se trata de una sustancia incolora, ligeramente higroscópica y altamente oxidante. Mezclado con sustancias orgánicas puede provocar explosiones. El nitrato es sólo ligeramente tóxico (LD50 = 1267 mg/kg rata) pero puede ser transformado en nitrito con actividades fisiológicas mayores y más dañinas.
Principales aplicaciones
- Como conservante en la industria alimenticia (E251) y en la mezcla de sales empleada para tratar la carne en su conservación.
- Fundido en mezcla con carbonato sódico en la obtención del cromo de sus minerales por oxidación de este metal a cromato. (CrO42-)
- Debido a su contenido en nitrógeno se utiliza como fertilizante.
- Como aditivo para el cemento.
- Debido a que al quemarse genera oxígeno, ha sido empleado en varias ocasiones a lo largo de la historia para conseguir un fuego que ardiese bajo el agua, como es el caso del fuego griego.
- Es uno de los ingredientes mayoritarios de ciertos tipos de pólvora negra.
Resumen Histórico desde su Descubrimiento y Explotación
Los bosques del Tamarugal intervinieron de una manera directa e inmediata en la creación de la industria salitrera y fomentaron, con detrimento propio, su vasto y rápido desarrollo.
En el último tercio del siglo XVIII, los elaboradores del nitrato de soda es fama que se cobijaban en los espesos bosques de la Tirana, como alquimistas perseguidos, para cocer el caliche clandestinamente, y extraer de él esa valiosa sustancia que aplicaba con tan buen éxito a la fabricación de la pólvora, en oposición al Rey de España, que la tenía monopolizada y la expendía en sus estancos y factorías.
La tradición conserva el nombre de Mariano Ollero como uno de los indígenas que trabajaban con más empeño, a fines del siglo XVIII, en el beneficio del salitre. Extraían de ciertos sitios poco distantes, piedras cubiertas con salitre, y en cuyo interior se hallaban vetas de la misma sustancia. Entre los elaboradores por tradición, de ese período, se en encuentran los siguientes, algunos de ellos indígenas: Esteban Vernal, Benito Calla, Manuel Hidalgo, José Jacinto Plaza, Manuel Arias, Vicente Granadino, Bacilio Carpio, Atanacio Tinaxas. También figura el nombre de una mujer, doña Anda Vilca.
Elaboración
Una vez extraído el caliche y luego departido en trozos menudos, su lixiviación se hacía cociéndolo con agua dentro de un fondo o un par de fondos de cobre, los cuales eran calentados a fuego vivo mediante una hornilla o fogón, el que, colocado debajo o entre los dos fondos, permitía darle calefacción a ambos. Con el aumento de la temperatura a que estaba sometida la masa en el interior de los fondos, se precipitada el cloruro de sodio y el agua iba saturándose cada vez mas del nitrato de sodio, lográndose así la separación de las distintas sustancias. Una vez disueltas éstas, el líquido saturado con las mismas -llamado aguas madres- pasaba a otro depósito donde era clarificado y terminaba cristalizándose. Cuando el salitre, que primeramente se encontraba en estado de solución, se cristaliza, es un grumo perfectamente blanco, de olor característico y que conserva humedad, debiendo ser expuesto a la intemperie para secarse.
Este primer sistema de elaborar el nitrato de sodio, conocido posteriormente con el nombre de Paradas, se utilizó hasta la segunda mitad del siglo XIX, siendo frecuentemente reformado. Los fondos de cobre que se usaban eran los mismos que empleaban los españoles en el tratamiento de los minerales de plata y no cabe duda que fueron los mineros españoles los primeros elaboradores del salitre de Tarapacá, siendo eficazmente secundados por los indígenas que realizaban las mismas operaciones en diversos lugares de la Pampa del Tamarugal utilizando pequeñas pailas.
Industria del Nitrato de Sodio
A mediados de 1830 el salitre fue comprado en Francia y Estados Unidos, casi enseguida en Inglaterra y mas tarde en Alemania, Italia y otros países europeos. El comienzo de la exportación de salitre al Viejo Mundo marca el hito más importante en la historia de la industria salitrera. La industria del nitrato empezó a recibir nuevos impulsos a partir de la década de 1850. La provincia de Tarapacá contó con un mayor contingente de trabajo y capital expresados en la afluencia de hombres de empresa, en su mayoría extranjeros y principalmente chilenos. Además, en este período (1953) se implantó un procedimiento técnico para elaborar el salitre basado en la disolución del caliche por medio del vapor de agua, sistema debido al inventor chileno don Pedro Gamboni, gracias al cual surgieron las primeras oficinas dotadas de máquinas a vapor y con capacidad de producción incomparablemente superior a las del sistema de Paradas.
Hasta 1866 el yodo había sido una sustancia desaprovechada en la Pampa Salitrera. El mismo industrial e inventor chileno logró, después de largas experiencias, constituir un procedimiento para la extracción del yodo de las aguas madres y solicitó la patente y el privilegio legal para explotarlo. En ese mismo año, otro hecho de trascendental importancia para el desarrollo de la industria del salitre tuvo lugar fuera del territorio peruano cuando el industrial y explorador chileno don José Santos Ossa, realizaba con éxito ante el gobierno de Bolivia las gestiones legales para explorar salitre en él.
En Octubre de 1869 se inició la elaboración de salitre en la oficina Salar del Carmen, la primera planta productora de nitrato que se instalaba fuera del territorio peruano, al sur del río Loa. El primer ferrocarril salitrero, inaugurado a mediados de 1871, se estableció para unir el puerto de Iquique con el cantón de La Noria. Se estableció así una nueva era en el transporte salitrero, iniciándose el reemplazo de los antiguos caminos de herradura.
Hacia 1890 y poco después, alrededor del 60% de la industria del nitrato estaba controlada directa o indirectamente por las sociedades anónimas que tenían su asiento en Londres. En los años siguientes, sin embargo, se observó un incremento de inversiones chilenas y alemanas y en adelante empezó a declinar la preponderancia de la influencia inglesa, quedando en proporción con la chilena en la primera década del siglo XX. En 1912 y considerando la producción conjunta de las dos provincias, Tarapacá y Antofagasta, los intereses chilenos representaban cerca del 40% y alrededor del 60% los de otras nacionalidades. La exportación superaba los dos millones de toneladas por año.
Asociación de Productores de Salitre de Chile
Uno de los aspectos al que no se le dio importancia suficiente en los primeros tiempos era la propaganda del producto, no obstante que para cumplir ese fin se formó en 1886 un Comité Salitrero Permanente. Una mejor organización de los medios, para dar a conocer el fertilizante en las instituciones agrícolas y agronómicas extranjeras, se estableció en 1884 al fundarse la Asociación Salitrera de Propaganda, la cual se convirtió en la Asociación de Productores de Salitre de Chile en 1919. En el curso de la década de 1870 el ingeniero inglés don Santiago Humberstone logró, después de largos estudios, concluir un sistema de elaboración basado igualmente en el empleo del vapor agua, pero en forma indirecta, en tubos cerrados, y con un nuevo tipo de cachuchos de gran capacidad de contenido y provistos en su interior de serpientes de tubos, por los que pasaba el vapor para calentar la masa de caliche y agua en tratamiento. Los cachuchos adaptados por el Sr. Humberstone para la elaboración del salitre se basaban en los del Sistema Shanks empleado en Inglaterra para la elaboración de la soda.
La mayor parte de la producción se realizaba todavía en Tarapacá, donde casi la totalidad de los cantones salitreros habían estado en explotación desde antes de la guerra. Entre la primera y la segunda década del siglo XX la producción empezó a ser reforzada con el creciente aumento de las explotaciones en las regiones de El Toco, Antofagasta, Aguas Blancas y Taltal.
Desde 1910 estos distritos del Sur competían con la antigua provincia salitrera del Norte y poco después de 1912 Antofagasta superaba a Iquique como puerto de exportación. La industria ocupaba en esos años más de 45 mil trabajadores, de los cuales 21 mil estaban localizados en las salitreras de Tarapacá. Según el censo de 1907, la población salitrera de las dos provincias había sido ese año de 36.700 trabajadores.
Nitratos y Nitritos
Muchos alimentos de consumo diario y especialmente las carnes procesadas, son conservados con estos tóxicos químicos. Se utilizan en la carne para resaltar el color rojo y hacer que aparente más apetecible a la hora de comprar. Inclusive los alimentos para bebés contienen nitratos.
Igualmente, los fertilizantes con nitratos frecuentemente utilizados hoy, contaminan el ganado y el agua del grifo o manantial, ríos etc. Cuanto más se utilizan fertilizantes de nitratos, especialmente en la maduración final de la planta, tanto mayor cantidad de nitrato aparece en los alimentos y agua del grifo.
Algunas plantas de hojas verdes, como en el caso de la espinaca, acumulan cantidades elevadas de nitrato. Lo mismo ocurre con raíces como la remolacha y la zanahoria. La única forma en que se puede evitar esto es mediante los métodos de agricultura biológica. Aún así, el agua con que se riega y los abonos de los animales que están a su vez contaminados, pueden aportar nitratos a un cultivo biológico o a un huerto familiar. Claro que el grado de contaminación es menor pero es casi imposible en la actualidad escaparse de esta trampa mortal. Cuando las hortalizas crecen a la sombra, como sucede a menudo en las zonas cálidas, el nivel de nitratos todavía aumenta más en el alimento y a la vez disminuye el contenido de vitamina C.
Las aguas residuales de ciudades, pueblos y zonas agrícolas, aumentan aún más la carga de nitratos contenida en el agua de riego o en el agua potable del grifo, las fuentes y manantiales.
La función principal de los nitratos es dar a las carnes envejecidas, y a veces en descomposición, un saludable y optimista tono rosado o rojizo y reforzar su sabor. La pura necesidad de recurrir a estos aditivos queda reflejada en el ejemplo de los perros calientes o en las hamburguesas, pues sin ellos ningún consumidor comería esa mezcla de sebo, cereales, agua, soja texturizada y carnes de animales como cabras viejas o pollos enfermizos. Es sólo mediante el uso de nitratos que se puede conservar durante varias semana estos cadáveres.
Utilización como aditivos
Este insidioso veneno se añade a propósito a los comestibles más típicos y algunos alimentos. De hecho, bajo un nombre supuestamente inocente El de aditivos se esconde una cruda realidad:
- E 247 nitrito de potasio
- E 250 nitrito de sodio
- E 251 nitrato de potasio
- E 252 nitrato de sodio
Todas estas variedades tienen un denominador común: el ser destructores de los glóbulos rojos, tener la capacidad de provocar accidentes vasculares y ser potencialmente cancerígenos.
Como fertilizante
Nitrato de Sodio
LEY: 15.5 a 16% de N, 35% de sosa (26% de Sodio) y unos 30 oligoelementos. Esta riqueza corresponde al Nitrato sódico de Chile, mientras que los nitratos sintéticos noruegos se caracterizan por no contener oligoelementos.
Es un tipo de abono simple, nitrogenado, nítrico. Su aspecto cuando está puro es blanco. Su olor ligeramente acre recuerda al cal yodo. Su densidad según el apelmazamiento, 100 kg de nitrato sódico de Chile ocupan de 80 a 90 litros. Es fácilmente soluble en agua. A 0 ºC, 100 litros de agua disuelven 73 kg de nitrato sódico y a 20 ºC, 100 litros pueden disolver 88 kg de nitrato sódico.. La higroscopicidad: a 20 ºC es 22.9. A 30 ºC es 27.0. El nitrato sódico cristalizado moja los dedos. Absorbe fácilmente la humedad del aire. Se le considera de reacción neutra (índice de neutralización es 29). Aunque es neutro, actúa fisiológicamente como un producto alcalino que reduce las pérdidas de cal. Su salinidad es de índice elevado, aunque inferior al del cloruro sódico. Su principal acción negativa consiste en la acción dispersiva y defloculante de las arcillas.
El Nitrato Sódico de Chile: se obtiene de los depósitos Naturales de Chile. La roca madre de los nitratos sódicos de Chile, el caliche, parda, terrosa, incrustada de facetas brillantes, se extiende sobre inmensas superficies con un espesor de 0.5 a 3 m de las regiones desérticas de la parte septentrional de Chile. El yacimiento todavía unas 300 millones de toneladas de abono. Sobre el origen de estos depósitos existen diversas teorías. El Nitrato Sódico Sintético (fabricado en Noruega) se obtiene por la síntesis, debido a la acción del ácido nítrico sobre el carbonato sódico.
El nitrato sódico sólo puede mezclarse con el cloruro potásico y el superfosfato, en el momento de utilizarlo, puede mezclarse de antemano con las escorias, los fosfatos naturales y el fosfato bicálcico. El nitrato sódico debe conservarse al resguardo de la humedad.
El nitrato sódico sólo puede mezclarse con el cloruro potásico y el superfosfato, en el momento de utilizarlo, puede mezclarse de antemano con las escorias, los fosfatos naturales y el fosfato bicálcico. El nitrato sódico debe conservarse al resguardo de la humedad.
Síntomas de envenenamiento
Los síntomas de envenenamiento por estos aditivos pueden ser : asma, dolor de cabeza, Hipertensión, hipotensión, mareos, náuseas, desoxigenación de la sangre y colapso circulatorio, pulso irregular, vértigos, debilidad muscular, gastroenteritis con dolor abdominal y en experimentos con animales de laboratorio llevados a cabo en la Universidad de California, se comprobó que pequeñas cantidades de nitritos producen una amnesia anterógrada ( olvido de algo aprendido hace poco ).
Si después de una comida con embutidos experimentas dolores de cabezas, náuseas, disneas o vómitos, es probable que sea debido a una ligera intoxicación por nitritos presentes en cantidades muy elevadas en este tipo de alimento.
Las industrias que procesan la carne dependen de este para hacer que sus productos parezcan frescos a los ojos del consumidor. Esto es debido a que el nitrato imita el color de la carne. Lo que ocurre es que las bacterias en la carne actúan sobre el nitrato y lo reducen a nitrito. Y es justamente ese nitrito el que realiza la tarea de disfrazar el aspecto de la carne y mantenerla así. con lo cual estas industrias desprecian olímpica y temerariamente la realidad de que el nitrito es muchísimo más peligroso y tóxico que el nitrato. Naturalmente, la etiqueta del envase sólo citará a una E con la consabida cifra o nitrato sódico, pero de lo que sí puede estar seguro el consumidor es que cuando se va a consumir el producto envasado, buena aparte de ese nitrato. ¡se habrá convertido en el aún más peligroso nitrito
Otros peligros
Junto con la Hipertensión, el mayor peligro de los nitratos está en su potencial cancerígeno. De hecho, se trata de uno de los más potentes cancerígenos capaces de provocar cáncer de hígado, riñón, cerebro, pulmón, estómago, intestino, esófago, lengua, vejiga y nariz. Existen muy pocas sustancias cancerígenas que ataquen tantos órganos como lo hacen las nitrosaminas.
Las nitrosaminas son unas sustancias que se forman en el organismo por la ingestión de nitritos y aminas secundarias, que son en extremo, tóxicas y cancerígenas. El nitrito, una vez llegado al estómago, se combina con unas sustancias denominadas aminas secundarias, y se forman unos compuestos llamados nitrosaminas vía el proceso de la nitrosación. Las aminas secundarias están muy presentes en nuestra dieta desde el pescado, especialmente de mar, a los cereales y pasando por una simple taza de té negro.
Esta reacción química tiene lugar hasta cierto punto cuando se procesan las carnes, continúa mientras se expone en los escaparates y estanterías, y se acelera especialmente cuando se cocina. Sin embargo, aún puede favorecerse más si se someten estos ingredientes a una solución ácida, como por ejemplo... el jugo gástrico del estómago humano.
Alimentos que contienen nitratos
- Leche, sobre todo en polvo.
- Embutidos y productos de charcutería en general (carnes curadas, chorizo, jamón, perros calientes, salchichas, hamburguesas)
- pizzas de salchichón y de anchoas, especialmente si se consumen con vino o cerveza.
- Agunos dulces snacks, desayunos y alimentos bajos en grasa, contienen altos niveles de sodio a pesar de que no tienen un sabor salado.
- Conservas animales ( anchoas, jamón york, patés.)
- Conservas vegetales
- Agua del grifo
- Productos derivados de la soja, especialmente los que imitan a los productos cárnicos ( salvo los de cultivo biológico)
- Cerveza, vino, whisky, etc
- Leche y quesos
- Patatas, espinacas, acelgas, pepinos, berenjenas, zanahorias, remolacha roja y raíces en general
- Sandía Cómerlas sólo en plena temporada
- Aguas minerales (una vez abierta la botella se debe conservar en el frigorífico o consumir el contenido lo más rápido posible si no, notará un olor terrible)
Precauciones en la manipulación
- No es combustible pero facilita el incendio si se pone en contacto con otras materiales combustibles originando peligro de incendio y explosión. En caso de incendio desprende humos (o gases) tóxicos
- Si se dispersa el polvo puede provocar tos, dificultad respiratoria y es necesario aire limpio, reposo y proporcionar asistencia médica respiratoria. La sustancia irrita los ojos, la piel y el tracto respiratorio.
- Para su manipulación se deben utilizar guantes protectores, pues puede provocar enrojecimiento de la piel, en este caso se debe aclarar con agua abundante,
- Después de manipular esta sustancia es necesario bañarse con abundante agua, no comer, beber ni fumar antes de bañarse.
- La sustancia puede causar efectos en la sangre, dando lugar a la producción de metahemoglobina. Los efectos pueden aparecer de forma no inmediata. Se recomienda vigilancia médica.
Fuentes
- http://ponce.inter.edu/cai/reserva/jvelazquez/aditivos.html
- http://cambiaelmundodespiertate.wordpress.com/tag/nitrato-de-sodio/
- http://micocinavegetariana.com/descubren-altos-niveles-de-sodio-en-alimentos-bajos-en-grasa/
- http://www.biomanantial.com/aditivos-conservantes-alimentos-a-952-es.html
- http://www.quiminet.com
- http://www.buenastareas.com/ensayos/Conservadores-y-Colorantes-En-Los-Alimentos/50777.html
- http://www.lenntech.es/periodica/elementos/be.htm
- http://www.albumdesierto.cl/historia.htm