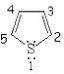
Tiofeno
| ||||||
Tiofeno. Es un compuesto orgánico, heterocíclico y aromático con fórmula C4H4S. Se encuentra en el petróleo y presenta su estructura en forma de anillo plano de cinco miembros. Produce CO2, H2O y SO2 en la combustión completa. Relacionados al tiofeno existe el benzotiofeno y el dibenzotiofeno, que contienen el anillo de tiofeno unido a uno o dos anillos de benceno respectivamente. Otros compuestos análogos al tiofeno son el furano y el pirrol.
Sumario
Abundancia en la naturaleza
El tiofeno fue descubierto como un contaminante en el benceno. Se observó que la isatina forma una tinta azul cuando es mezclada con el ácido sulfúrico y benceno crudo. La formación del azul indofenina se adjudicó durante mucho tiempo a una reacción con el benceno. Victor Meyer, fue el primero en aislar la sustancia responsable de esta reacción desde el benceno. Este nuevo compuesto heterocíclico fue el tiofeno.
El tiofeno y sus derivados se encuentran en el petróleo, a veces en concentraciones de 1-3%, específicamente en el alquitrán de hulla. El tiofeno contenido en el petróleo y en el carbón es extraído mediante el proceso de hidrodesulfuración (HDS). En la HDS, el líquido o el gas pasa sobre un catalizador de disulfuro de molibdeno bajo presión de H2.
Los tiofenos experimentan además hidrógenolisis para formar hidrocarburos y sulfuro de hidrógeno. De esta forma, el tiofeno se convierte en butano y H2S. Aunque en el petróleo se encuentra mayor cantidad de benzotiofeno y dibenzotiofeno.
Diversas plantas sintetizan tiofenos con actividad nematicida, como es el caso del α-tertienilo producido por asteráceas del género Tagetes.
Propiedades físicas
El Tiofeno se conoce con otros nombres como Tiofurano y Tiaciclopentadieno y a temperatura ambiente, es un líquido incoloro con un débil olor agradable, dentro de las propiedades físicas más notables:
- Fórmula empírica: C4H4S
- Masa molecular : 84,14 g/mol
- Estado físico: Líquido
- Color: Incoloro
- Número CAS: 110-02-1
- Densidad: 1,051 g/cm3 a 20 °C
- Punto de fusión: -38,0 °C (187,6 K)
- Punto de ebullición: 84,0 °C (304,4 K)
- Solubilidad en agua: 0 g/l a 25 °C.
El tiofeno posee algunas similitudes al benceno.
Estructura
La molécula de Tiofeno, es plana; el ángulo de enlace en el azufre es de unos 93º, el ángulo C-C-S es de alrededor de 109º y los otros dos carbonos poseen un ángulo de enlace de 114º. Las longitudes de los enlaces C-C adyacentes al azufre son de 1.34A, la longitud del C-S es de 1.07A y el otro C-C es de 1.41A.
Propiedades químicas
El tiofeno es considerado aromático, aunque los cálculos teóricos sugieren que el grado de aromaticidad es menor que el del benceno. Los pares electrónicos del azufre están significativamente deslocalizados en el sistema π. Como una consecuencia de su aromaticidad, el tiofeno no exhibe las propiedades típicas de los tioéteres. Por ejemplo, el átomo de azufre, resiste la alquilación y la oxidación. Cuando se somete el análisis de los productos de la combustión, una muestra de 1,086g de tiofeno produce 2,272g de CO2, 0,465g de H2O y 0,827g de SO2. La alta reactividad del benceno hacia la sulfonación constituye la base para la separación del tiofeno del benceno. Separación que resulta complicada para realizar mediante destilación debido a sus puntos de ebullición similares (4ºC de diferencia a presión ambiente). Como el benceno, el tiofeno forma un azeótropo con el etanol.
Reactividad frente a diversos grupos de compuestos
- Frente a electrófilos
Aunque el átomo de azufre es muy poco reactivo, los carbonos adyacentes (carbonos 2 y 5), son altamente susceptibles al ataque de electrófilos. Los halógenos dan inicialmente 2-halo derivados seguidamente dando, 2,5-dihalotiofenos; la perhalogenación es fácilmente alcanzable dando C4X4S (X = Cl, Br, I). Thiophene brominates 107 times faster than does benzene.
La clorometilación y la cloroetilación ocurre fácilmente en las posiciones 2 y 5. La reducción del producto clorometilo da 2-metiltiofeno. La hidrólisis seguida de deshidratación de los productos cloroetílicos da 2-viniltiofeno.
- Desulfuración con níquel Raney
La desulfuración del tiofeno con Níquel Raney proporciona butano. Cuando se acopla a la 2,5-difuncionalización del tiofeno, la desulfuración constituye una vía para obtener butanos 1,4-disustituidos.
- Litiación
No solamente frente a electrófilos es reactivo el tiofeno, también es fácilmente litiado con n-butil-litio para dar 2-litiotiofeno, el cual es un precursor para muchos otros derivados como el ditienil.
- Química de coordinación
El tiofeno exhibe un comportamiento similar al del tioéter, pero sirve como un ligando pi formando complejos tipo taburete de piano como Cr(η5-C4H4S)(CO)3.
- Politiofeno
El polímero formado por la unión entre tiofenos a través de las posiciones 2,5 es llamado politiofeno. El politiofeno en sí mismo posee pobres propiedades de procesamiento. Más útiles son los polímeros derivados de los tiofenos sustituidos en las posiciones 3- y 4-. Los politiofenos se tornan conductores eléctricos luego de una oxidación parcial (se convierten en 'metales orgánicos').
Obtención
El tiofeno es pruducido en una escala de aproximadamente de dos millones de kilos por año mundialmente. La producción involucra una reacción en fase gaseosa entre una fuente de azufre, normalmente disulfuro de carbono y n-butanol. Estos reactivos se ponen en contacto con un catalizador de óxido a 500-550 ºC.
Como un reflejo de sus estabilidades, los tiofenos se forman desde muchas reacciones que involucran fuentes de azufre e hidrocarburos, especialmente aquellos insaturados por ejemplo: acetilenos y azufre elemental. La cual fue la primer síntesis de tiofeno realizada por Viktor Meyer en el año de su descubrimiento.
Los tiofenos son preparados por la reacción entre 1,4-dicetonas, diésteres o dicarboxilatos con reactivos sulfurantes como P4S10. Tiofenos más específicos pueden ser sintetizados utilizando el reactivo de Lawesson como agente sulfurante o mediante la Reacción de Gewald, que involucra la condensación de dos ésteres en presencia de azufre elemental. Otro método es la Ciclación de Volhard-Erdmann.
Aplicaciones
Los tiofenos son importantes compuestos heterocíclicos muy usados ampliamente como ingredientes en muchos agroquímicos y drogas. El anillo de benceno de un compuesto biológicamente activo puede ser muchas veces reemplazado por un tiofeno sin pérdida de actividad. Esto se observa, por ejemplo, en las drogas antiinflamatorias no esteroideas (NSAID) como el lornoxicam, el análogo de tiofeno del piroxicam.
Efectos sobre el medio ambiente y la salud
- Altamente inflamable. En caso de incendio se desprenden humos (o gases) tóxicos e irritantes. Es necesario evitar las llamas, noproducir chispas y no fumar. No poner en contacto con agentes oxidantes. Espuma, polvo, dióxido de carbono.
- Explosión: Las mezclas vapor/aire son explosivas. Sistema cerrado, ventilación, equipo eléctrico y de alumbrado a prueba de explosión. Evitar la generación de cargas electrostáticas (por ejemplo, mediante conexión a tierra). En caso de incendio: mantener fríos los bidones y demás instalaciones rociando con agua.
Sobre la salud
- Tos. Dolor de garganta; Debe existir ventilación, extracción localizada o protección respiratoria. Aire limpio y reposo.
- Piel. Enrojecimiento; usar guantes protectores, quitar las ropas contaminadas, aclarar y lavar la piel con agua y jabón.
- Ojos. Enrojecimiento, dolor; Usar gafas ajustadas de seguridad, o protección ocular combinada con la protección respiratoria.
- Ingestión; no comer, ni beber, ni fumar durante el trabajo, enjuagar la boca y reposo.
De ocurrir derrrames y escapes de Tiofeno. Recoger, en la medida de lo posible, el líquido que se derrama y el ya derramado en recipientes herméticos. Absorber el líquido residual en arena o absorbente inerte y trasladarlo a un lugar seguro. No verterlo al alcantarillado. (Protección personal adicional: filtro respiratorio para vapores orgánicos y gases).
Derivados de tiofeno
Se refiere a derivados de tiofeno, su preparación y su uso como compuestos farmacéuticamente activos. Dichos compuestos actúan particularmente como agentes inmunosupresores. Reivindicación 1: Un compuesto seleccionado del grupo formado pro tiofenos de la fórmula (1), donde:
- R1, representa metilo, trifluorometilo, o etilo;
- R2 representa hidrógeno, alquilo C1-4, metoxi, o halógeno;
- R3 representa hidrógeno, alquilo C1-4, alcoxi C1-4, o halógeno;
- R4 representa hidrógeno, alquilo C1-4, o halógeno;
- R5 representa hidrógeno;
- R6 representa hidrógeno o hidroxi;
Cuando R6 representa hidroxi, R5 puede también representar hidroxi; n representa 0; m representa 0 o 1; y cuando m representa 1, n puede también representar 1; y sales así como complejos solventes de tales compuestos.
Fuentes
- B. Pavlov, A Terrrentiev .Curso de Química Orgánica traducido por Victoria Valdez Mendoza Editorial Mir Moscú 1970 pag. 471.
- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A.. ISBN 84-282-0882-4.
- [1]
- Sustancias quimicas
- Derivados de tiofeno