Mioglobina
| ||||||
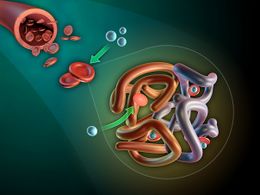
Mioglobina. Es una proteína sarcoplásmica, responsable del transporte y almacenamiento del oxígeno dentro del tejido muscular.
Estructura
La mioglobina está formada por una sola cadena polipeptídica unida a un grupo hemo. Fue la primera proteína de la que se determinó su estructura tridimensional, en 1957, un hito de la bioquímica por lo que Jonh Kendrew, recibió el premio Nobel.
La estructura de la mioglobina es muy compacta, con alrededor del 75 % de la cadena plegado en forma de hélices a, con una estructura cuaternaria mantenida sobre todo por enlaces hidrofóbicos. El grupo hemo se sitúa en una oquedad de la molécula.
Las mayores concentraciones de mioglobina se encuentran en el músculo esquelético y en el músculo cardíaco, donde se requieren grandes cantidades de oxígeno para satisfacer la demanda energética de las contracciones.
Grupo hemo
El grupo hemo consta de una parte orgánica y un átomo de hierro. La parte orgánica es la protoporfirina y está formada por cuatro grupos pirrólicos. Los cuatro pirroles están unidos por medio de puentes meteno para formar un anillo tetrapirrólico. A este anillo están enlazados cuatro metilos, dos vinilos y dos cadenas laterales de propionato.
El átomo de hierro del hemo está ligado a los cuatro nitrógenos en el centro del anillo de la protoporfirina. El hierro puede formar otros dos enlaces, uno a cada lado del plano del hemo. Estos lugares se denominan la quinta y sexta posición de coordinación. La quinta posición se coordina con un residuo de histidina en la hélice F de la hemoglobina (histidina proximal), mientras que la sexta posición es ocupada por el oxígeno. Cerca de donde se une el oxígeno al grupo hemo, existe otra histidina (histidina distal) que previene que otras moléculas de hemoglobina entren en contacto produciendo la oxidación del Fe2+ a Fe3+ y disminuye la afinidad de la hemoglobina por el Monóxido de Carbono (CO). El átomo de hierro del hemo puede estar en estado de oxidación ferroso (+2) o férrico (+3). Las formas correspondientes de la hemoglobina se denominan ferrohemoglobina y ferrihemoglobina (o metahemoglobina), respectivamente. Solamente la ferrohemoglobina (+2) puede captar oxígeno.
Mioglobina y el color de la carne
La mioglobina es el principal pigmento de la carne, y el color de este producto depende fundamentalmente del estado en el que se encuentra la mioglobina.
En el músculo, el hierro se encuentra en la mioglobina en forma de ión ferroso, y así se encuentra también en la carne fresca. El grupo hemo puede tener asociada una molécula de oxígeno, formando entonces la oximioglobina, de color rojo brillante, que es el que se observa en la parte exterior de la carne.
En el interior, la mioglobina no tiene oxígeno unido, estando entonces en forma de desoximioglobina, que tiene un color rojo púrpura más intenso y oscuro que el de la oximioglobina. Estas dos formas son interconvertibles, dependiendo de la presión parcial de oxígeno, y en la práctica, de la superficie de contacto.
En las condiciones de una atmósfera normal, el ion ferroso es inestable, pasando a ion férrico. En la mioglobina, la presencia del grupo hemo y de la cadena de proteína lo protegen, pero aún así, la oxidación se produce con cierta rapidez, especialmente si la superficie de contacto es grande, como en el caso de la carne picada.
La mioglobina con el hierro en forma férrica recibe el nombre de metamioglobina o ferrimioglobina, y tiene un color marrón poco atractivo, el de la carne almacenada demasiado tiempo. Este proceso es reversible, por la acción de un enzima, la metamioglobin-reductasa, en presencia de agentes reductores.
En la oxidación de la mioglobina se puede formar superóxido, que puede dar lugar a reacciones de oxidación de lípidos:
Mb-Fe2+O2 → Mb-Fe3+ + O2•-
El color de la carne depende también del pH alcanzado en el proceso de maduración, y la velocidad a la que se alcanza. Sin embargo, esta variación en el color no tiene relación estrictamente con la mioglobina, sino con la textura de las fibras musculares y la forma en la que reflejan y refractan la luz.
Si se calienta la carne, en el cocinado, la parte proteica de la mioglobina se desnaturaliza rápidamente, permitiendo la oxidación del hierro y produciendo el ferrihemocromo, que tienen el color marrón de la carne cocinada.
En los productos curados, el óxido nítrico (NO), procedente de la reducción de los nitritos utilizados como aditivo, se une al hierro de la mioglobina, dando nitrosilmioglobina, pigmento de color rojo, pero relativamente inestable. La desnaturalización de la proteína permite que se una al hierro un segundo NO, que estabiliza el color formando ferrohemocromo.
Funciones
Sirve como un reservorio y acarreador de Oxígeno, incrementando la velocidad de transporte del mismo en la célula muscular, es decir facilita la difusión del oxígeno desde los capilares hasta el interior de las células (mitocondrias) que está limitada por la baja solubilidad del oxígeno en soluciones acuosas.