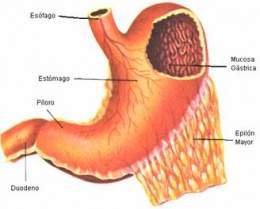
Mucosa gástrica
| ||||||
Mucosa gástrica. Revestimiento del estómago, que consiste en un epitelio interno, una membrana mucosa media y una muscularis mucosae externa. Las células superficiales producen moco que proteje al estomago del ataque de ácidos y enzimas digestivas. Cuando el epitelio se invagina dentro de la membrana mucosa en varias regiones del estómago, se forman diferentes glándulas gástricas tubulares. Estas glándulas están constituidas`por células que secretan moco, enzimas, ácido clorhídrico y hormonas.
Sumario
Mecanismos defensivos de la mucosa
Los endógenos y exógenos es debida a un número de procesos defensivos que operan dentro y alrededor de la mucosa.
Capa estable de Moco y Bicarbonato
La primera línea de defensa de la mucosa es la capa estable formada por el gel mucoso y el bicarbonato que cubren la superficie luminal mucosa y así mantienen un microambiente neutro en las células superficiales epiteliales. Además de ser parte de la capa estable, el moco sirve como lubricante, retarda la difusión de hidrogeniones y pepsina, inhibe la activación del pepsinógeno y ejerce una acción antibacteriana. Un grupo de hormonas gastrointestinales como la gastrina y secretina; la prostaglandina E2 y agentes colinérgicos estimulan la secreción de moco. También algunos medicamentos activos tópicamente (tal como los antiácidos) estimulan la secreción de moco.
El bicarbonato es secretado al lumen por células epiteliales superficiales y parcialmente por células parietales estimuladas ("marea alcalina"). El gel mucoso minimiza la pérdida luminal de bicarbonato manteniendo así un microclima neutro en la superficie mucosa.
La secreción de bicarbonato es estimulada por las prostaglandinas y compuestos con aluminio (Ej. antiácidos).
Células Epiteliales superficiales
La segunda línea de defensa mucosa está formada por la capa continua de células epiteliales superficiales que segregan moco y bicarbonato (contribuyendo a la capa estable) y generan prostaglandinas. Debido a la presencia de fosfolípidos en su superficie, estas células son hidrofóbicas, repeliendo el ácido y agentes dañinos hidrosolubles. Interconectados por uniones firmes (o rígidas), las células superficiales epiteliales forman una "barrera" que previene la retrodifusión de ácido y pepsina.
Renovación Celular
La continua renovación celular, desde células progenitoras en la zona proliferativa mucosa, produce el reemplazo de células superficiales dañadas o viejas. Estas células progenitoras en la zona del cuello de la glándula, expresan receptores para el factor de crecimiento epidérmico y péptidos relacionados, como el factor de crecimiento transformante alfa que son los principales factores de crecimiento responsables de esta proliferación celular. Usualmente lleva de 3 a 5 días reemplazar completamente el epitelio superficial. Más tiempo (meses) toma reemplazar las células glandulares. La injuria superficial al epitelio mucoso es restituida en algunas horas por medio de la migración de células del área del cuello.
"Marca Alcalina"
Las células parietales secretantes de HCI al lumen gástrico en forma simultanea secretando bicarbonato dentro del lumen de la microvascularidad adyacente. De allí el bicarbonato es transportado hacia la porción superior de la foveola contribuyendo al microclima neutro en la superficie luminal.
Microcirculación
La microcirculación mucosa libera oxígeno y nutrientes a la mucosa completa y remueve sustancias tóxicas. El endotelio microvascular genera vasodilatadores tales como la prostaciclina y el óxido nítrico (NO), que protegen a la mucosa gástrica contra la injuria y se oponen a la acción dañina de la mucosa de los vasoconstrictores, como leucotrieno C4' tromboxano A2 y endotelina. Cuando la microvasculatura está dañada, las células endoteliales de la microvascularidad periférica a las áreas lesionadas inician la reparación y reconstrucción de la trama microvascular a través de la angiogénesis.
Prostagiandinas
La generación permanente de prostaglandinas E2 (PGE2) y prostaciclina (PGI2) por la mucosa es crucial para mantener la integridad de la mucosa. Casi todos los mecanismos defensivos de la mucosa son estimulados o facilitados por prostaglandinas exógenas o endógenas. La inhibición de la síntesis de prostaglandinas por agentes antiinflamatorios no esteroideos o la neutralización de las prostaglandinas endógenas por anticuerpos específicos resultan en la formación de úlceras gástricas e intestinales.
Nervios Sensoriales
La estimulación de nervios sensoriales gástricos conduce a la liberación de neurotransmisores como el péptido relacionado al gen de la calcitonina (PRGC) y la sustancia P en las terminaciones nerviosas, localizados dentro o cerca de los grandes vasos subrnucosos. PRGC ejerce una acción protectora de la mucosa más probablemente a través de la vasodilatación de los vasos submucosos vía la generación de óxido nítrico. Además, macrófagos de la mucosa, leucocitos y células endoteliales secretan una gama de citoquinas que afectan el crecimiento celular y su proliferación.
Matrix Extracelular
La matrix extracelular y sus componentes específicos tales como fibronectina, laminina, y colágeno proporcionan un soporte estructural para las células epiteliales y endoteliales, y juegan un importante rol en la adherencia, migración, proliferación y diferenciación celular. La matrix extracelular está compuesta por células (fibroblastos, miofibroblastos), glucosaminoglicanos (proteoglicanos unidos a proteínas ácido hialurónico no ligado a proteínas y heparina), proteína fibrilares tales como colágenos y elastina y glicoproteínas no filamentosas (fibronectina, laminina, entactina, ondulina y otros).
Hasta hace poco la matrix extracelular se consideraba como meramente una trama extracelular para sostener las células epiteliales. Trabajos recientes indican que la matrix extracelular juega un rol activo en las funciones de la mucosa. Se ha reconocido que los componentes de la matrix extracelular están unidos a través de integrinas con el citoesqueleto celular permitiendo la transferencia bidireccional de información respecto a la forma de la célula y su crecimiento. Fijación celular, migración, proliferación y diferenciación. La matrix extracelular está compuesta de componentes que conducen comunicación a las células respecto a cambios en su ambiente. Estos componentes permiten la interacción de la matrix extracelular con el epitelio gástrico mucoso y las células endoteliales.
Factores agresivos
La mucosa gástrica está constantemente expuesta a numerosos factores agresivos exógenos y endógenos.
Factores agresivos como el ácido clorhídrico (HCI) y la pepsina están presentes dentro del lumen gastrointestinal y son importantes para la digestión inicial del alimento. El HCI en particular está suficientemente concentrado (más de 2 millones de veces que el pH tisular) para dañar el tejido; pero bajo circunstancias normales la mucosa gastroduodenal está protegida por sus propios mecanismos de defensa. Además los ácidos biliares y la lisolecitina, que refluyen a menudo del duodeno, pueden potencialmente dañar la mucosa gástrica.
Además de los factores endógenos, la mucosa gastroduodenal es sujeto de ataque de un número de agentes exógenos ingeridos: antiinflamatorios no esteroideos (AINES), como aspirina e indometacina; alcohol y agentes quimioterapéuticos. Todos ellos causan erosiones gástricas, sangrado y ulceraciones. Además de estos agentes el Helicobacter pylori, comúnmente encontrado en el estómago humano, produce varias toxinas capaces de dañar la mucosa gástrica. El fumar actúa como un factor agresivo al reducir el flujo sanguíneo de la mucosa gástrica, inhibiendo la producción de prostaglandinas mucosas y aumentando el reflujo de bilis dentro del estómago desde el duodeno.
Fisiopatolgía del daño mucoso gastroduodenal
Cuando la mucosa gástrica se expone a agentes lesivos como la aspirina, indometacina, ácidos biliares, toxinas del Helicobacter pylori o a factores necrotizantes como alcohol, isquemia o agentes corrosivos, la mucosa desarrolla modificaciones morfológicas, ultra estructurales y funcionales ante la injuria. El desarrollo y extensión de la injuria mucosa depende de la naturaleza y concentración del agente gastrolesivo.
Como está representado en la Figura 2, la injuria aguda de la mucosa gástrica consiste de (1) disrupción de la capa estable y la superficie hidrofóbica, (2) injuria y exfoliación de la superficie epitelial con pérdida de su barrera y función eléctrica, (3) injuria de capas más profundas de la mucosa gástrica incluyendo: (a) células endoteliales microvasculares, (b) zona de células progenitoras y (c) células parietales y principales. El daño del endotelio microvascular conduce al estasis microvascular, cesación del suministro de oxígeno, del transporte de nutrientes y de ahí a una necrosis por isquemia. El daño microvascular ocurre tempranamente durante la injuria mucosa, precede a la necrosis de las células glandulares y añade un componente isquémico a la injuria tóxica directa de estas células. Los cambios vasculares (por ej. constricción de las venas) producidos por la liberación de mediadores vasoactivos pro inflamatorios de las células dañadas (mastocitos, macrófagos y células endoteliales) comprometen adicionalmente la microcirculación y finalmente resulta en necrosis mucosa.
La disrupción de la capa estable, la superficie hidrofóbica y la exfoliación del epitelio superficial con pérdida de su función de barrera permite a agentes ulcerogénicos y a factores agresivos penetrar la mucosa para liberar mediadores vasoactivos y proinflamatorios y exagerar la estasis microvascular posterior y/o el daño celular directo y los componentes de tejido conectivo de la mucosa. Todos estos eventos resultan en la formación de erosiones o ulceraciones de la mucosa. La diferencia entre una erosión y una úlcera es que la primera está confinada a la mucosa mientras una úlcera penetra a la muscularis mucoide.
Protección de la Mucosa por Antiáciados
Desde el descubrimiento del ácido clorhídrico en las secreciones gástricas una premisa del tratamiento de la úlcera péptica ha sido que la neutralización del ácido podía conducir a la curación de las úlceras. Los antiácidos se convirtieron en una elección terapéutica lógica y la investigación en la farmacología de los antiácidos se convirtieron en una elección terapéutica lógica y la investigación en la farmacología de los antiácidos se centró principalmente en su capacidad neutralizante del ácido. La neutralización del ácido se ha pensado y asumido como el único mecanismo de las acciones protectora y curativa de los antiácidos.
Los antiácidos han mostrado en suma su efectividad para cicatrizar úlceras duodenales y gástricas; pero algo muy interesante, la terapia antiácida a dosis bajas con una capacidad neutralizante pequeña (120-200 mmol/día) parece ser tan efectiva como una dosis mucho mayor (cinco veces) de antiácidos. Los antiácidos se ha encontrado que son más efectivos que los antagonistas H2-histamina en prevenir las úlceras inducidas por el estrés y el sangrado. Estos hallazgos indican que la acción curativa y protectora de los antiácidos puede ser independiente de sus propiedades antineutralizantes.
- La citoprotección se refiere a la habilidad de prostaglandinas y otros compuestos para proteger la mucosa contra varios agentes necrotizantes (incluyendo el alcohol absoluto) por mecanismos diferentes a la inhibición o neutralización de la secreción de ácido gástrico. El concepto de la citoprotección pone especial énfasis en los mecanismos defensivos de la mucosa gástrica, Las propiedades de la citoprotección han sido reclamados como propios por varios fármacos usados en el tratamiento de la enfermedad ulcerosa péptica, incluyendo los antagonistas H2-histamina como la cimetidina y la ranitidina. Los antagonistas H2 histamina pueden dar protección contra lesiones inducidas o facilitadas por el ácido pero son completamente inefectivas en la protección de la mucosa gástrica producida por agentes necrotizantes tales como el alcohol concentrado o la distensión gástrica.
Varios estudios han demostrado que los antiácidos son capaces de proteger la mucosa gástrica contra la injuria producida por indometacina, aspirina, HCI 0.6, NaOH 0.2 M. taurocolato sódico y etanol concentrado. Pero el análisis detallado de los aspectos histológicos, ultraestructurales y funcionales de la protección y su secuencia en el tiempo falta en la mayoría de estos estudios.
Se ha demostrado que los antiácidos que contienen aluminio reducen la necrosis de la mucosa gástrica inducida por el etanol.
Este tipo de injuria es independiente del ácido luminal y no fue reducido aún utilizando dosis muy altas de cimetidina, ranitidina, famotidina, nizatidina y omeprazol. El pretratamiento con antiácido redujo significativamente la necrosis de la mucosa gástrica inducida por el alcohol, la extensión de la necrosis histológica profunda y disminuyó las pérdidas sanguíneas y de proteínas intragástricas. Todos estos aspectos de la protección de la mucosa gástrica por antiácidos fueron similares a la citoprotección de la mucosa gástrica por prostaglandinas. En un estudio aparte encontramos que el antiácido acidificado (con HCI) es 8-10 veces más efectivo que el antiácido regular en proteger a la mucosa de la injuria por alcohol. La acción protectora del Hidróxido de Aluminio: Hidróxido de Magnesio 650: 350 acidificado indica que el mecanismo de protección de la mucosa por este antiácido es enteramente independiente de su habilidad para neutralizar el ácido luminal y de allí que tiene todas las propiedades de la citoprotección. En un estudio preliminar hemos demostrado que este antiácido protege la mucosa gástrica contra la injuria producida por el NaOH 0.2 M y a la mucosa duodenal contra la necrosis inducida por el alcohol.
En los más recientes estudios nosotros demostramos que Hidróxido de Aluminio: Hidróxido de Magnesio 650: 350 efectivamente protege contra la injuria producida por el alcohol. Reduce significativamente el puntaje de injuria evaluado endoscópicamente, también la necrosis histológica profunda, la injuria al endotelio microvascular y a los componentes de la matrix extracelular.