Plasma rico en plaquetas
| ||||||
Plasma rico en plaquetas. El plasma rico en plaquetas es un concentrado de plaquetas obtenido del plasma del propio paciente, el cual contiene enormes reservas de proteínas bioactivas, incluidos factores de crecimiento y células madre periféricas, que son de vital importancia para iniciar y acelerar la reparación tisular.
Sumario
Historia
El plasma rico en plaquetas(PRP) tiene sus antecedentes en 1994 cuando ungrupo de cirujanos empleó la adición de un adhesivo de fibrina autógena al hueso esponjoso durante la reconstrucción mandibular. Para ello recurrieron a la separaciçon de una muestra de sangre en sus componentes y emplearon la fracción plasmática como crioprecipitado. Observaron una consolidación ósea precoz. Más adelante Marx y Cols, observaron que el PRP aumentaba la concentración de plaquetas en los injertos , observándose la presencia de al menos tres factores de crecimiento:Factor de crecimiento de origen plaquetario(PDGF), Factor de crecimiento de transformación beta-1 y 2 (TGF-β1 y β2).
Obtención
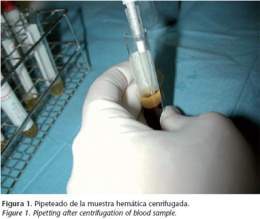
Para la obtención del PRP se realiza la extracción de sangre total. La cantidad de sangre necesaria dependerá de las áreas a tratar, la cual será procesada en el servicio de banco de sangre mediante centrifugación y desplasmatización para obtener el superconcentrado de plaquetas. Luego se procede a su activación, para lo cual se añaden 0.05 cc de cloruro cálcico al 10% por cada 1 cc de plasma rico en plaquetas y factores de crecimiento. Todo este proceder bajo condiciones de flujo laminar, para evitar la contaminación del producto final.
Utilización
Se utiliza en la regeneración de tejido óseo, muscular,ligamentario, fibras de colágeno, y vasos sanguíneos; en especialidades como ortopedia y traumatología, angiología, cirugía estética y maxilofacial.Su utilización constituye un avance en el tratamiento de diversas enfermedades que se relacionan por especialidades a continuación:
- Ortopedia y traumatología:
Tendinitis y ruptura del tendón de Aquiles
Injerto del ligamento cruzado anterior
Epicondilitis
Lesiones musculares y de meniscos
Pubalgias
Lesiones condrales en rodilla y tobillo
Pseudoartrosis
Retraso de consolidación
- Odontología:
Alvéolo postextracción
Colocación de implantes en hueso tipo III y IV
Colocación inmediata de implantes
Levantamiento de piso de seno
Relleno de defectos óseos
Tratamiento periodontal
Comunicaciones bucosinusales
Fístula buconasal
- Angiología:
Arterioesclerosis obliterante de los miembros inferiores
Úlceras vasculares
Úlcera del pie diabético
- Cirugía estética:
En Inyección Subdérmica (surcos pronunciados, cicatrices, fibrosis).
En adición a material adipocitario (como injerto).
En lipotransferencia enriquecida por PRP (arrugas, surcos, aumento o remodelación de pómulos, labio o mentón)
En paniculopatía edemato-fibro-esclerótica (celulitis).
Aplicación
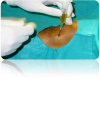
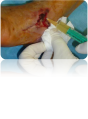
Se aplica en forma líquida en las infiltraciones intra-articulares, lesiones tendinosas y en las musculares. Para las heridas, se obtiene un coágulo rico en factores de crecimiento que es maleable y fácilmente aplicable en una zona concreta.
Fundamentos de la capacidad terapéutica del plasma
Lasplaquetas son células sanguíneas anucleadas derivadas de megacariocitos que tienen la propiedad de adherirse a las paredes vasculares dañadas formando agregados; su vida media es de 7-10 días y sus valores normales oscilan entre 150 y 450 x 10 9/mm3. Tras su activación, liberan de sus gránulos proteínas llamadas citocinas. Algunas de estas citocinas que se comportan como señalizadoras y regulan procesos celulares clave como la diferenciación, la mitogénesis y la quimiotaxis reciben el nombre de Factores de Crecimiento (FC). Se han descrito un gran número de estas proteínas, pero en el tema que nos ocupa los más importantes son PDGF (Growth factor derived from platelets) TGF-B (Transformed beta growth factor), FGF (Fibroblast growth factor), VEGF. (Vascular endothelial growth factor), e IGF (Insulin-Growth factor).
El coágulo de fibrina del PRP actúa como primordio del nuevo tejido y de vehículo del reclutamiento celular y vascular. Va a ser substituido progresivamente por matriz extracelular propia del tejido afectado que es producida a partir de la diferenciación celular mediada por factores del ambiente.
Las señales recibidas a través de las citocinas propias del tejido dañado van a conducir a la diferenciación tejido específica. En este sentido juegan un importante papel la acción de FC como TGF-ß, bFGF, EGF, HGF y el IGF-1.
A continuación, coexistiendo con el proceso de la fibrinolisis y la activación endotelial, se produce la liberación .in situ. de FC secretados por los gránulos α plaquetarios que han quedado secuestrados en el interior de la malla de fibrina. Este .kit. disparador químico desempeña el papel de desencadenante de la respuesta regenerativa. El principal Factor de Crecimiento que hace de bisagra en estas respuestas es el TGF-ß que se secreta en dos formas:
a) Forma latente en complejos pequeños de acción inmediata que promueven la atracción de células inmunitarias y que son degradados por las enzimas .furin-like. liberadas por las mismas plaquetas.
b) Forma latente de liberación tardía, formando complejos grandes ligados a la matriz extracelular fibrilar (o a la propia fibrina) por medio del LTBP (.latent TGF binding protein.) degradada fundamentalmente por la plasmina en el momento de la fibrinolisis y que desencadena la respuesta regenerativa propiamente dicha. En este momento la acción del TGF-ß es fundamentalmente antiinflamatoria.
La regeneración de un tejido exige la formación de nuevos vasos sanguíneos. La angiogénesis va a ser el motor de la regeneración desde el inicio ya que posibilitará la llegada de células tronco multilineales y proporcionará factores tróficos necesarios para la homeostasis celular. El inicio de la angiogénesis se desencadena por la esfingosina-1-fosfato (SPP), también liberada por las plaquetas, que se une al receptor EDG-1 de las células endoteliales ejerciendo una acción quimioatrayente sobre las mismas. Un cofactor, que parece ser la fibronectina, estabiliza la interacción de la célula endotelial con la matriz extracelular.
La acción subsiguiente viene mediada fundamentalmente por el VEGF (FC vasculoendotelial) que actúa como factor inductor de la proliferación de las células endoteliales y movilizador de células progenitoras de sistema vascular para promover la vasculogénesis. Esta respuesta coordinada a escala local y sistémica producirá un nuevo árbol vascular en la zona dañada gobernando la formación del nuevo tejido.
Asegurado el aporte vascular, se forma un tejido intermedio de origen fibroso que actúa a modo de nicho que albergará a las células progenitoras movilizadas por los mediadores del daño celular que llegan al foco de lesión guiadas por gradientes químicos y anidan en el .homing. Normalmente, la célula stem queda regulada en su nicho, que es otra célula de aspecto fibroblástico. En respuesta a estímulos mitógenos va a producir progenitores y precursores de forma ordenada que se encargarán de sustituir el primordio de tejido (tejido fibroso de granulación) por el tejido noble.
Factores de crecimiento presentes en el PRP:
- PDGF:
Promueve indirectamente la angiogénesis a través de los macrófagos, por un mecanismo de quimiotaxis. Activador de macrófagos. Mitógeno de células mesenquimales. Facilita la formación de colágeno tipo I.
- TGF-BETA:
Quimiotaxis.
Proliferación y diferenciación de las células mesenquimales.
Síntesis de colágeno por los osteoblastos.
Pro-angiogénesis.
Inhibe la formación de osteoclastos
Inhibe la proliferación de células epiteliales en presencia de otros factores.
- FGF:
Proliferación y diferenciación de los osteoblastos.
Inhiben los osteoclastos.
Proliferación de fibroblastos e inducción de la secreción de fibronectina por estos.
Pro-angiogénesis por acción quimiotáctica sobre células endoteliales.
- IGF:
Proliferación y diferenciación de células mesenquimales y de revestimiento.
Síntesis de osteocalcina, fosfatasa alcalina y colágeno I por los osteoblastos.
- VEGF:
Quimiotaxis y proliferación de células endoteliales
Hiperpermeabilidad de los vasos sanguíneos.
Posibes riesgos
Los autores que han empleado clínicamente el PRP aseguran que no existen riesgos de infección o transmisión de enfermedades y niegan la existencia de algún tipo de efecto indeseable, y no existe ningún caso en la literatura que muestre resultados de este tipo. Sin embargo, se ha relacionado la sobreexpresión de factores de crecimiento y sus receptores con tejidos tumorales y displásicos, lo cual hace pensar en dos posibles peligros: la carcinogénesis y la posibilidad de favorecer la metástasis. Es cierto que existen empíricamente estos riesgos pero no existe ningún caso descrito en la literatura, y los concentrados terapéuticos de FC como el PRP podrían actuar como promotores, no como iniciadores en la carcinogénesis, pero este fenómeno necesitaría de dosis mayores y más continuadas en el tiempo que las que se aplican en la terapéutica convencional.
Fuentes
- Revista Española de Cirugía Oral y Maxilofacialversión.2006[citado 2012 septiembre ,10 ]; Disponible en: scielo.isciii.es
- Revista Internacional de Odontología Restauradora & Periodoncia, 2002;[citado 2012 septiembre ,10 ]; Disponible en:europa.sim.ucm.es
- Revista Internacional de Odontología Restauradora & Periodoncia, 2002[citado 2012 septiembre ,10 ]; Disponible en:europa.sim.ucm.es
- Aplicación de Adhesivo Plaquetario Autólogo:Mejora cicatrizaciónen pacientes quemados. 2002[citado 2012 septiembre ,10 ]; Disponible en:www.cienciaytrabajo.
- Reconstrucción de la mama con gel de plaquetasen la cirugía conservadora del cáncer.2012[citado 2012 septiembre ,10 ]; Disponible en:www.sciencedirect
- Plasma rico en plaquetas: ¿un nuevo tratamiento para el reumatólogo?.2012[citado 2012 septiembre ,10 ]; Disponible en: www.sciencedirect.com
- Anales de medicina interna.2002[citado 2012 septiembre ,10 ]; Disponible en:http://scielo.isciii.es