Diferencia entre revisiones de «Anión hidróxilo»
(→Fuente) |
|||
| (No se muestran 9 ediciones intermedias de 3 usuarios) | |||
| Línea 1: | Línea 1: | ||
| + | |||
{{Definición | {{Definición | ||
|nombre=Anión hidróxilo | |nombre=Anión hidróxilo | ||
| Línea 4: | Línea 5: | ||
|tamaño= | |tamaño= | ||
|concepto=OH<sup>-</sup> | |concepto=OH<sup>-</sup> | ||
| − | }}'''Anión hidróxilo'''. Ion formado por un [[ | + | }}'''Anión hidróxilo'''. Ion formado por un [[átomo]] de [[oxígeno]] y un atómo [[hidrógeno]] y su carga eléctrica es -1.También llamado ion oxhidrilo. |
== Aniones == | == Aniones == | ||
| Línea 18: | Línea 19: | ||
*Sn(OH)4: Tetrahidróxido de estaño ! [[Hidróxido de estaño]] (IV) | *Sn(OH)4: Tetrahidróxido de estaño ! [[Hidróxido de estaño]] (IV) | ||
== Fuente == | == Fuente == | ||
| − | * | + | *Salas Tort, Dolores. Nomenclatura de Compuestos químicos. Revista Cubana de Química. [[Universidad de Oriente]].[[2007]] |
| + | == Ver también == | ||
| + | *[[Química inorgánica]] | ||
[[Category:Química inorgánica]] | [[Category:Química inorgánica]] | ||
última versión al 01:01 30 jun 2020
| ||||||
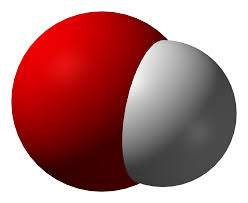
Anión hidróxilo. Ion formado por un átomo de oxígeno y un atómo hidrógeno y su carga eléctrica es -1.También llamado ion oxhidrilo.
Aniones
Se llaman aniones a las “especies químicas” cargadas negativamente. Los aniones más simples son los monoatómicos, que proceden de la ganancia de uno o más electrones por un elemento electronegativo.
Aniones poliatómicos
Los aniones poliatómicos se pueden considerar como provenientes de otras moléculas por pérdida de uno o más iones hidrógeno. El ion de este tipo más usual y sencillo es el ion hidroxilo (OH–) que procede de la pérdida de un ion hidrógeno del agua.
Compuestos químicos
Se trata de compuestos por un catión metálico y el anión hidróxido (OH-). Para formularlos ponemos primero el catión y luego tantos hidróxidos como sea necesario para igualar las cargas.
Ejemplos
- Hidróxido de cobre (II): Cu2+(OH-)2 ! Cu(OH)2
- Trihidróxido de hierro: Fe(OH)3
- Dihidróxido de cobalto: Co(OH)2
- Sn(OH)4: Tetrahidróxido de estaño ! Hidróxido de estaño (IV)
Fuente
- Salas Tort, Dolores. Nomenclatura de Compuestos químicos. Revista Cubana de Química. Universidad de Oriente.2007