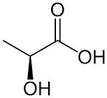
Ácido láctico
| ||||||
Ácido láctico. Producto intermedio del metabolismo, principalmente del ciclo de los carbohidratos y deriva principalmente de las células musculares. Este producto orgánico, ocurre naturalmente en el organismo de un ser humano. Además de ser un producto secundario del ejercicio, también es un combustible para ello. Se encuentra en los músculos, la sangre, y varios órganos.
Sumario
Historia
Fue descubrimiento por el químico sueco Scheele, en 1780, se orginó cuando aisló la leche agria, fue reconocido como producto de fermentación por Blonodeaur en 1847, y tan solo en 1881, Littlelon inicia la fermentación a escala industrial. Es un compuesto muy versátil utilizado en la industria química, farmacéutica, de alimentos y de plásticos.
Existen dos isómeros ópticos, el D (-), láctico y el L (+) láctico y una forma racémica constituida por fracciones equimolares de las formas D (-) y L (+). A diferencia del isómero D(-), la configuración L(+) es metabolizada por el organismo humano. Ambas formas isoméricas del ácido láctico pueden ser polimerizadas y se pueden producir polímeros con diferentes propiedades dependiendo de la composición.
Comportamiento
En el organismo siempre hay pequeñas cantidades de ácido láctico en la sangre que oscilan entre 4,5 a 19,8 mg/dl o como se suele usar en el mundo del deporte (0,5-2,2 mmol/L). Cuando se activa el proceso de obtención de energía por medio de la Glucólisis anaeróbica unos de los resultados es la creación de este ácido. Esta molécula vuelve a ser absorbida por el organismo, principalmente por el hígado. La fórmula química es C3 H6 O3 y fue descubierto en 1780.
Importacia biológica
El ácido ℓ-láctico se produce a partir del piruvato a través de la enzima lactato deshidrogenasa (LDH) en procesos de fermentación. El lactato se produce constantemente durante el metabolismo y sobre todo durante el ejercicio, pero no aumenta su concentración hasta que el índice de producción no supere al índice de eliminación de lactato. El índice de eliminación depende de varios factores, como por ejemplo: transportadores monocarboxilatos, concentración de LDH y capacidad oxidativa en los tejidos.
La concentración de lactatos en la sangre usualmente es de 1 o 2 mmol/l en reposo, pero puede aumentar hasta 20 mmol/l durante un esfuerzo intenso. El aumento de la concentración de lactatos ocurre generalmente cuando la demanda de energía en tejidos (principalmente musculares) sobrepasa la disponibilidad de oxígeno en sangre.
Bajo estas condiciones la piruvato deshidrogenasa no alcanza a convertir el piruvato a acetil~CoA lo suficientemente rápido y el piruvato comienza a acumularse. Esto generalmente inhibiría la glucólisis y reduciría la producción de Adenosín trifosfato (ATP, sirve para acumular energía), si no fuera porque la LDH reduce el piruvato a lactato: piruvato + NADH + H+ --> lactato + NAD+ El proceso de la producción de lactato es regenerar la dinucleótido adenina nicotinamida (NAD+) necesario para la glucólisis y entonces para que continúe la producción de ATP. El incremento de lactato producido puede eliminarse de diversas formas: la oxidación a piruvato en las células musculares bien oxigenadas, que es usado directamente para completar el ciclo de Krebs y convertir la glucosa a través del ciclo de Cori. La fermentación de ácido láctico también la produce las bacterias Lactobacillus.Estas bacterias pueden encontrarse en la boca, y puede ser el responsable de la creación de caries.
Propiedades
- Fórmula: C3H6O3
- Peso molecular: 90,08
- Índice de refracción: 1,4414
- Punto de fusión: L(+) y D(-) 52,8 a 54 ºC
- Punto de ebullición: 125-140 ºC
- Gravedad específica: 1206
- Calor de combustión: 3616 cal/g
- Viscosidad: 40,33 mNsm-2
- Densidad: 1,249
- Constante dieléctrica: 22ε
Usos y especificaciones
Los derivados como sales y ésteres son ampliamente utilizados en la industria alimenticia, química, farmacéuticas, del plástico, textil, la agricultura, alimentación animal entre otros. En la industria alimenticia se usa como acidulante y conservante. Las industrias químicas lo utilizan como solubilizador y como agente controlador de pH.
En la producción de pinturas y resinas, puede ser utilizado como solvente biodegradable. En la industria de plásticos es utilizado como precursor del ácido poliláctico (PLA), un polímero biodegradable con interesantes usos en la industria y la medicina; se considera ésta la principal aplicación del ácido y por la cual a aumentado considerablemente la demanda.
Fermentación láctica
- A partir del azúcar de la leche (lactosa)con el Bacillus lactis acid
- A partir de almidón, azúcar de uva (glucosa) o azúcar de caña(sacarosa) utilizando el Bacillus Delbrücki
La obtención de ácido láctico con enzimas o microorganismos vivos pueden producir isómeros dextrógiros o levógiros, dependiendo de la enzima involucrada en el proceso.
Causas que producen aumento del ácido láctico
- Hipertensión
- Sépsis y neoplasias
- Anemia aguda
- Cetoacidósis diabética
- Deshidratación grave
- Intoxicación alcohólica aguda
- Insuficiencia hepática grave
- Insuficiencia respiratoriacon hipóxia grave
- Shock
- Isquemia regionales del cuerpo como es en el infarmo mesentérico o la izquemia de extremidades por Embolia.
- Ejercicio excesivo
- Intoxicación por Monóxido de Carbono
Véase también
Fuentes
- Ácido lácticotodonatacion.comConsultado el 20 de febrero de 2012.
- Producción biotecnológica de ácido láctico eis.uva.esConsultado el 20 de febrero de 2012.
- Ácido lácticocuidar-su-salud.blogspot.comConsultado el 20 de febrero de 2012.
- Ácido láctico wikipedia.org
- Ácido 2-hidroxi-propanoicolaanunciataikerketa.comConsultado el 20 de febrero de 2012.