Trichinella
| ||||||||||
Trichinella es el género de gusanos parásitos, común al hombre y a numerosas especies de mamíferos, provocada por el enquistamiento de larvas de Trichinella spiralis en la musculatura estriada del corazón, el sistema musculoesquelético, el cerebro o el tracto gastrointestinal.
Sumario
Introducción
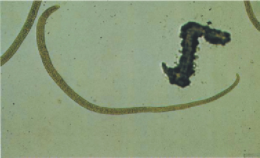
Trichinella es un nemátodo intestinal pequeño, blanquecino y filiforme con la extremidad posterior engrosada. La mayoría de las personas infectadas permanecen asintomáticas y no están severamente afectadas, aunque en otras puede llegar a ser mortal. La enfermedad es adquirida por el consumo de carne infectada mal cocida o cruda, por lo general de cerdo, en zonas templadas, y de animales salvajes en los polos y los trópicos. Tiene mayor incidencia en las regiones templadas que en las tropicales. Es cosmopolita, se encuentra en varios continentes, inclusive en la región ártica, aunque es más frecuente en países de Asia, de África y de América Latina.
Clasificación taxonómica
De acuerdo con la nomenclatura, existen ocho tipos distintos de especies, cada una de las cuales fue designada con un número, por ejemplo: Trichinella spiralis se designó como T1. Otras especies solo han tenido nominaciones númericas: T5, T6 y T8. La combinación de ADN tipaje y de patrones izoenzimáticos ha sido usada para identificar especies responsables de infecciones selváticas y humanas.
1. Reino: Animalia
2. Phyllum: Nematodo
3. Subclase: Adenophorea
4. Orden: Enoplida
5. Superfamilia: Trichuroidea
6. Familia: Trichinellidae
7. Género: Trichinella
8. Especie: spiralis con las siguientes variedades: spiralis, nativa, britovi, nelsoni y pseudospiralis.
Agente etiológico
Trichinella spiralis es un nematodo intestinal pequeño, blanquecino y filiforme con la extremidad posterior engrosada. Las hembras adultas miden de 2 a 4 mm de largo por 75 a 90 mm de ancho, cerca del doble de longitud y una y media veces del ancho del macho. La boca es inerme, se continúa con el tubo esofágico y el intestino, que termina en la cloaca en el macho y en el ano en la hembra. Los dos tercios posteriores del parásito corresponden al aparato reproductor en los dos sexos, el cual es muy simple. El macho presenta en su extremo posterior dos papilas cónicas que utiliza para la cópula. No hay espícula. La hembra es vivípara y puede observarse con larvas en el interior del útero. Los huevos, esféricos, miden 20 mm de diámetro; las larvas, 100 mm, a diferencia de las que se establecen en los músculos, que pueden alcanzar hasta 1 mm de longitud. En los músculos, cada larva se enrolla sobre sí misma y forma un quiste ovalado de 250 a500 mm. Se han propuesto designaciones taxonómicas separadas para las especies del Ártico (Trichinella nativa) y el Paleoártico (Trichinella britovi), de África (Trichinella nelsoni), y en zonas cosmopolitas del mundo (Trichinella pseudospiralis).
Ciclo de vida
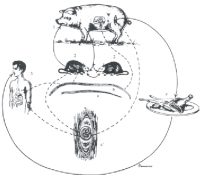
Existe muy poca especificidad de hospederos; prácticamente cualquier animal puede alojar tanto los parásitos como las formas larvarias, por lo cual se considera a estos animales infectados como hospederos definitivos e intermediarios al mismo tiempo. Los adultos copulan en el intestino: los machos mueren después de unas cuantas semanas, y son eliminados con las materias fecales, casi nunca llegan a observarse; pero las hembras grávidas permanecen en la mucosa. Las hembras penetran la mucosa del intestino delgado y producen larvas que alcanzan los capilares, y por el torrente sanguíneo llegan a los pulmones sin pasar a los alvéolos, siguen por la sangre y se diseminan por la vía arterial a todo el organismo. Pueden invadir pulmones, miocardio y encéfalo, de manera transitoria, allí son destruidas, pero dejan a su paso un proceso inflamatorio. Por un tropismo positivo hacia los músculos estriados, invaden la fibra muscular, crecen y se rodean de una envoltura, que al cabo de 1 mes está bien constituida para formar el quiste, el cual es un mecanismo de defensa del huésped, a la vez que es una protección para la larva. Esta puede permanecer viable por muchos años, en espera de ser ingerida por un nuevo huésped. Si esto no sucede, el quiste termina por recubrirse con sales de calcio y la larva muere. Cuando un nuevo hospedero ingiere larvas enquistadas viables, tal como sucede cuando el hombre come carne de cerdo mal cocida o el cerdo se alimenta de ratas infectadas, el quiste es digerido en el estómago, las larvas penetran la pared del intestino delgado en donde crecen y se transforman en parásitos adultos, que reinician el ciclo de vida (Fig.)
Fig. Ciclo de vida de Trichinella spiralis. Numerosos mamíferos actúan como hospederos definitivos e intermediarios al mismo tiempo. Los parásitos adultos, macho (a) y hembra (b) habitan normalmente el intestino delgado de su hospedero: cerdo (1), rata (2), hombre (3) y otros. Después de la cópula, la hembra se introduce en la mucosa intestinal donde pone sus embriones que ganan el torrente circulatorio y se dirigen a los músculos de los mismos hospederos, que actúan a la vez de hospederos definitivos e intermediarios. Llegados a los músculos, se enquistan, para allí producir larvas (c`). El cerdo generalmente se infesta por ingestión de desperdicios de otros cerdos infestados, más raramente de ratas contaminadas o de otros animales infestados. Las ratas se contaminan al devorarse unas a las otras, o al ingerir carne de cualquier otro animal contaminado con las formas larvarias.
Manifestaciones clínicas
Al cabo de 3 ó 4 días de la ingesta de carne infestada, el paciente puede presentar síntomas de una gastroenteritis. Los síntomas corresponden a la fijación de las hembras fecundadas en la pared intestinal y se autolimitan en pocos días, aunque en ocasiones la diarrea puede persistir algunas semanas. La triquinosis casi siempre se divide en tres etapas clínicas: intestinal, invasión muscular y convalecencia. Durante el período de invasión muscular aparecen complicaciones miocárdicas o neurológicas. La mayoría de los pacientes presentan un cuadro diarreico muy semejante al que ocurre en una clásica intoxicación alimentaria aguda. Lo difícil para hacer el diagnóstico es pensar que se trata de una triquinosis, ya que es mucho más rara que una intoxicación alimentaria. Al final de la primera semana, que coincide con la migración larval, aparece con frecuencia fiebre, escalofríos, edema de la cara, fundamentalmente de los párpados superiores, mialgias, cefalea, hiperemia conjuntival, hemorragias subconjuntivales, retinianas y ungueales, fotofobia y diplopía. Con menor frecuencia se observa un exantema maculopapular y cierto grado de edema en el tronco y las extremidades. El dato más característico es la miositis, con mialgias espontáneas a la palpación y a la movilización de las masas musculares, así como rigidez y debilidad. El paciente puede referir disfagia, trismo, dolor torácico o periorbitario, en relación con mialgias de los músculos de la faringe, maseteros, diafragma, intercostales y extrínsecos del ojo. Las formas graves pueden evolucionar con miocarditis manifestada por taquicardia, hipotensión, alteraciones del electrocardiograma e insuficiencia cardíaca, así como afectación del SNC con cefalea, obnubilación, delirio y diversos signos focales. El LCR suele ser normal. A veces hay infección pulmonar, que puede ocasionar hemoptisis y signos de consolidación. La gravedad del cuadro descrito difiere mucho de un caso a otro y depende en gran medida del volumen de carne parasitada ingerida. Por término medio, el proceso dura unas 3 semanas, pero en casos graves puede persistir 2 meses o más. Menos de 10 % de los pacientes con manifestaciones clínicas fallecen a las 4 ó 6 semanas por complicaciones neurológicas, cardíacas o pulmonares.
Etapa intestinal
Puede estar ausente, pero si se presenta el inicio es repentino; comienza 2 a 7 días después de la infección. La diarrea y el dolor abdominal son predominantes, en ocasiones se acompaña de náuseas, distensión y sensación de plenitud. Vómito, fiebre y estreñimiento son poco comunes. Los hallazgos físicos son inespecíficos.
Etapa de invasión muscular
Comienza durante la segunda semana después de la infección. La fiebre y edema periorbital son seguidos por mialgias y debilidad. Son menos comunes las cefaleas, exantemas cutáneos, prurito y tos seca. Los escalofríos casi siempre preceden a la fiebre, que puede llegar a 40 °C o más y persistir por 10 semanas en un patrón remitente o intermitente. Hay aumento de la sensibilidad y dolor muscular, que es común, ya sea con el movimiento o en reposo. Cualquier músculo puede estar afectado, incluyendo los maseteros. La inflamación del músculo puede manifestarse con características nodulares o una diuresis difusa. La debilidad es importante y la inflamación puede causar dolor con el movimiento.
Los hallazgos oculares incluyen edema periorbital aproximadamente en tres cuartes partes de los pacientes, además de dolor, fotofobia, y conjuntivitis con edema y hemorragia. Se han informado casos de hemorragias retinianas. El rash cutáneo más común es una erupción macular fina, en particular sobre el tronco, que dura solo unos cuantos días. Puede haber erupciones de urticaria y petequias; se han observado prurito o sensación de hormigueo. Las hemorragias en astillas debajo de las uñas, en forma típica distales, se observan en cerca de dos tercios de los pacientes. También hay invasión del músculo cardíaco en la mayor parte de los individuos, pero son raros los síntomas. Cuando está presente la miocarditis, se manifiesta a la tercera semana de la infección y se caracteriza por palpitaciones, disnea, y opresión torácica. Tanto la taquicardia como la bradicardia pueden afectar al paciente, pero la primera es más común; las arritmias o insuficiencia cardíaca congestiva pueden llegar a la muerte. Es común la cefalea y la aparición de mareos. En infecciones graves aumenta la presión intracraneal, hay cambios de comportamiento, delirio, estupor, y coma, convulsiones, y signos neurológicos locales; también se han encontrado hemiparesias. Otros hallazgos incluyen tos seca, laringitis por edema laríngeo o disfagia por invasión de los músculos esofágicos. Es rara la muerte y casi siempre se debe a miocarditis, encefalitis, o complicaciones como neumonía lobar y septicemia.
Etapa de convalecencia
Después de 3 ó 4 semanas, la etapa de invasión muscular cambia hacia la de convalecencia, en la que el tiempo de la fiebre disminuye y se limita en forma gradual al dolor, debilidad y otros síntomas. La debilidad muscular puede persistir y en raras ocasiones, en casos graves, ser permanente. La recuperación clínica completa ocurre de 2 a 6 meses como regla general, pero persiste una eosinofilia de baja a moderada intensidad por algunos meses.
Diagnóstico
El antecedente de ingestión de carne de cerdo poco cocida, junto a la aparición de casos similares en otros comensales y el cuadro clínico característico, sobre todo en las formas graves, sugieren el diagnóstico. Existen varias anomalías biológicas que pueden apoyar este diagnóstico, entre las cuales se destacan:
- La aparición de leucocitosis con eosinofilia es el hallazgo principal, de forma casi constante. Su máximo de hasta 90 % se encuentra a partir de la segunda y cuarta semanas, y puede persistir elevada durante varios meses.
- Aumento de enzimas musculares.
- Durante la tercera semana de la enfermedad, pueden observarse hipoalbuminemia e hipergammaglobulinemia con aumento de la IgE.
Las pruebas serológicas son de mucha utilidad, pero no se vuelven positivas hasta la segunda o tercera semanas de la enfermedad y pueden persistir positivas durante varios años. Las pruebas de enzimoinmunoanálisis permiten detectar IgG, IgM e IgA, frente a Trichinella spiralis. De forma excepcional se encuentra el parásito en heces, sangre o LCR. En 90 % de los casos sintomáticos, a partir de la tercera semana pueden encontrarse larvas enquistadas en muestras de biopsia muscular obtenidas cerca de la inserción tendinosa del deltoides o de los gemelos. Las larvas calcificadas en general son demasiado pequeñas para poder identificarlas en radiografías por partes blandas. La intradermorreacción de Bachean puede hacerse positiva durante las primeras cuatro semanas. La prueba del látex aparece positiva después de 4 semanas de infección. La inmunofluorescencia indirecta también es de utilidad. Estas dos últimas son poco específicas, por lo cual se han remplazado por otras como la técnica de ELISA. La técnica de ELISA y la hemaglutinación indirecta son dos pruebas de mayor especificidad y sensibilidad, y se convierten en positivas a las 3 semanas de iniciada la infección. La prueba definitiva es la biopsia muscular (en especial pectoral, de preferencia en el sitio de inflamación por hipersensibilidad), aunque no siempre es necesaria.
En particular, en un brote, la combinación de fiebre, mialgias, y eosinofilia, puede ser suficiente para apoyar un diagnóstico tentativo de triquinosis, y ser confirmado después por las pruebas serológicas. La posibilidad de tener biopsias positivas es la más alta entre la quinta y la sexta semanas después de la infección. Sin embargo, cualquier biopsia puede ser presuntiva del diagnóstico y muestra la transformación basofílica en la fibra muscular (que precede a la miositis), y es definitiva cuando se encuentra la larva enrollada. Las biopsias falsas negativas se presentan en pacientes que tienen una infección leve o si el procedimiento se realiza demasiado temprano. Parte de la muestra debe examinarse con el microscopio por compresión con los portaobjetos, por digestión, y pospreparación de muchas secciones microscópicas seriadas. En ocasiones las biopsias solo muestran evidencias de miositis o angiítis.
A veces, en la realización de otras pruebas pueden observarse larvas en pedículos de sangre periférica durante la etapa invasiva. El examen de heces para encontrar los parásitos es casi siempre negativo. La orina puede mostrar proteínas elevadas. Las enzimas musculares como la fosfoquinasa, están elevadas, el electromiograma muestra disfunción miopática. La presión de LCR en algunas ocasiones está elevada, con número normal o ligeramente alto en el conteo celular (linfocitos), la glucosa es normal, así como las proteínas que también pueden estar un poco elevadas, se puede encontrar la larva en el LCR simplificado. La velocidad de sedimentación casi siempre es normal, lo que resulta una clave útil para el diagnóstico. Se observan anormalidades electrocardiográficas en cerca de 20 % de los casos y casi siempre son inespecíficas; puede haber irritabilidad ventricular, o bloqueo cardíaco de primer o segundo grados, o defectos de conducción interventricular.
Epidemiología y prevención
La distribución es mundial, pero la incidencia es variable y depende en parte de las prácticas relacionadas con la ingestión y preparación de la carne de cerdo o de animales salvajes, y de la medida en que se intensifica y notifica la enfermedad. Los casos positivos, cuando se presentan, suelen ser esporádicos y los brotes localizados. Algunos de ellos se han debido al consumo de embutidos caseros y de otros productos de carne de cerdo o carne de mamíferos árticos como zorros, osos, focas, etc.
Tratamiento
Debido a sus pocos efectos secundarios es probable que el mebendazol sea preferible al tiabendazol. El tratamiento se basa en lo siguiente:
- Destruir el parásito adulto mediante el empleo de mebendazol a 200 ó 400 mg tres veces al día por 3 días, o a 400 ó 500 mg tres veces al día por 10 días.
- Impedir las reacciones de hipersensibilidad en las formas graves de la enfermedad, con la administración de prednisona a la dosis de 0,5 a 1 mg/kg/día. Conviene limitar la utilización de glucocorticoides a períodos cortos, con el fin de no interferir en la respuesta inmunitaria y el enquistamiento de las larvas.
Tratamiento de sostén
En algunas ocasiones se administran corticosteroides para reducir con rapidez la fiebre y la mialgia. Se emplean junto con los antihelmínticos para impedir la larviposición. Algunos casos de enfermedad grave pueden requerir el reposo en cama, fluidos endovenosos, apoyo nutricional, control cardíaco, tratamiento físico y otras medidas de apoyo.
Enlaces relacionados
Fuentes
- Libro: Microbiología y Parasitología Médicas Tomo III por Dra. Alina Llop Hernández
- Microbiología y Parasitología Médicas