Diferencia entre revisiones de «Buteno»
| Línea 2: | Línea 2: | ||
|nombre=Buteno | |nombre=Buteno | ||
|imagen=Bute.jpeg | |imagen=Bute.jpeg | ||
| − | |nombre,simbolo,numero= | + | |nombre,simbolo,numero=C4, H, 8 |
|serie_quimica= | |serie_quimica= | ||
|grupo,periodo,bloque= | |grupo,periodo,bloque= | ||
| − | |densidad= | + | |densidad=2.72 kg/m3 gaseosa y 630 kg/m3 líquida |
|apariencia= | |apariencia= | ||
|Propiedades_atomicas= | |Propiedades_atomicas= | ||
| Línea 41: | Línea 41: | ||
====Síntesis==== | ====Síntesis==== | ||
| − | + | De ser termólisis del petróleo se puede obtener el 1-Buteno por reacción de [[etileno]] con [[tris-etilaluminio]] a aproximadamente 100 °C y 100 bar. (Síntesis de 1-alquenos según [[Mülheimer]]). La reacción se parece a la síntesis del [[polietileno]] en catalizadores de [[Ziegler-Nata]]. | |
====Aplicaciones==== | ====Aplicaciones==== | ||
| Línea 84: | Línea 84: | ||
Tras halogenación con cloro y doble eliminación de HCl se obtiene [[butadieno]] que se utiliza en la síntesis de caucho artificial. Como los demás butenos también puede ser polimerizado directamente. | Tras halogenación con cloro y doble eliminación de HCl se obtiene [[butadieno]] que se utiliza en la síntesis de caucho artificial. Como los demás butenos también puede ser polimerizado directamente. | ||
| − | == | + | == Temas relacionados == |
*[[Eteno]] | *[[Eteno]] | ||
*[[Propeno]] | *[[Propeno]] | ||
| Línea 93: | Línea 93: | ||
== Fuentes == | == Fuentes == | ||
| + | * Artículo [http://www.grupoprevenir.es/fichas-seguridad-sustancias-quimicas/0838.htm Buteno]. Disponible en "www.grupoprevenir.es". Consultado: 5 de agosto de 2011. | ||
| + | * Morrison, R. T. y Boyd, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, [[Estados Unidos]], [[1990]]. | ||
* Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones Eneva]]. | * Requena, L. Vamos a Estudiar Química Orgánica. ([[2001]]). [[Ediciones Eneva]]. | ||
| − | |||
* Soto, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996. | * Soto, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996. | ||
| − | * Vollhardt, K. P. C.: Química Orgánica. Ed. Omega. [[Barcelona]], | + | * Vollhardt, K. P. C.: Química Orgánica. Ed. Omega. [[Barcelona]], 1996. |
| − | |||
[[Category: Química]] | [[Category: Química]] | ||
[[Category: Química_orgánica]] | [[Category: Química_orgánica]] | ||
[[Categoría:Hidrocarburos_alifáticos]] | [[Categoría:Hidrocarburos_alifáticos]] | ||
Revisión del 15:03 24 nov 2011
| ||||||||||||||||
Buteno. Hidrocarburo gaseoso incoloro que se usa en síntesis química. Alqueno formado por 4 átomos de carbono y 8 átomos de hidrógeno. Nombre de los isómeros de olefina con la fórmula C4H8 (1-buteno y 2-buteno). Fue encontrado por primera vez en 1825 por Michael Faraday en el aceite de gas.
Sumario
Propiedades
- Fórmula: C4H8
- Fórmula desarrollada: CH2=CH-CH2-CH3
- Masa molecular: 56,11 g/mol
- Límites de explosividad: 1,6 - 10 % Vol en aire.
Isómeros de posición
1-buteno
Propiedades físico-químicas
- Fórmula: H2C=CH–CH2–CH3
- Punto de fusión: –185,3 °C
- Punto de ebullición: –6,26 °C
- Solubilidad en agua: 200 g/l
Síntesis
De ser termólisis del petróleo se puede obtener el 1-Buteno por reacción de etileno con tris-etilaluminio a aproximadamente 100 °C y 100 bar. (Síntesis de 1-alquenos según Mülheimer). La reacción se parece a la síntesis del polietileno en catalizadores de Ziegler-Nata.
Aplicaciones
- En la síntesis del butadieno para el caucho artificial.
- En la síntesis del 2-butanol por adición de agua en presencia de ácido.
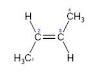
2-buteno
De este compuesto existen a su vez dos isómeros geométricos: Cis-2-buteno y Trans-2-buteno.
Propiedades físicoquímicas
| Propiedad | Cis-2-buteno | Trans-2-buteno |
|---|---|---|
| Fórmula | H3C–CH=CH-CH3 | H3C–CH=CH-CH3 |
| Temp. Fusión | –138,9 °C | –105,5 °C |
| Temp. Ebullición | 3,73 °C | 0,96 °C |
| Solub. en Agua | 5 g/l | 5 g/l |
Síntesis
Los 2-butenos se pueden obtener por metátesis en presencia de un catalizador a partir de propeno:
2 H3C–CH=CH2 → H3C–CH=CH–CH3 + H2C=CH2
Además de por pirólisis del petróleo. La reacción de eliminación a partir del 2-butanol suele dar mezclas de productos que contienen también los 2-butenos.
Aplicaciones
Tras halogenación con cloro y doble eliminación de HCl se obtiene butadieno que se utiliza en la síntesis de caucho artificial. Como los demás butenos también puede ser polimerizado directamente.
Temas relacionados
Fuentes
- Artículo Buteno. Disponible en "www.grupoprevenir.es". Consultado: 5 de agosto de 2011.
- Morrison, R. T. y Boyd, R. N.: Química Orgánica. Addison-Wesley Iberoamericana, S. A. Wilmington. Delaware, Estados Unidos, 1990.
- Requena, L. Vamos a Estudiar Química Orgánica. (2001). Ediciones Eneva.
- Soto, J. L.: Química Orgánica. Vol. I. Conceptos básicos. Ed. Síntesis, 1996.
- Vollhardt, K. P. C.: Química Orgánica. Ed. Omega. Barcelona, 1996.