Diferencia entre revisiones de «Displasia cortical»
(Etiqueta: nuestro-nuestra) |
(corrijo) (Etiqueta: nuestro-nuestra) |
||
| (No se muestran 2 ediciones intermedias del mismo usuario) | |||
| Línea 1: | Línea 1: | ||
{{Sistema:Moderación_Salud}} | {{Sistema:Moderación_Salud}} | ||
| + | |||
{{Enfermedad | {{Enfermedad | ||
| − | |nombre=Displasia | + | |nombre = Displasia cortical focal |
| − | |imagen_del_virus= Dcf0.jpg | + | |imagen_del_virus = Dcf0.jpg |
| − | |tamaño= | + | |tamaño = |
| − | |descripción= | + | |descripción = |
| − | |imagen_de_los_sintomas= | + | |imagen_de_los_sintomas = |
| − | |tamaño2= | + | |tamaño2 = |
| − | |descripción2=Malformaciones de la corteza cerebral | + | |descripción2 = Malformaciones de la corteza cerebral |
| − | |clasificacion= | + | |clasificacion = neurología |
| − | |region_de_origen= | + | |region_de_origen = |
| − | |region_mas_comun= | + | |region_mas_comun = cerebro |
| − | |agente_transmisor= | + | |agente_transmisor = |
| − | |forma_de_propagacion= | + | |forma_de_propagacion = malformación genética |
| − | |vacuna= | + | |vacuna = |
}} | }} | ||
| − | |||
| − | |||
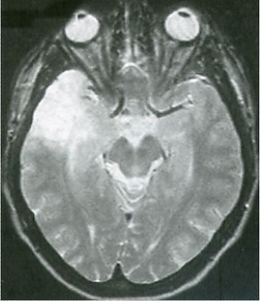
| − | La displasia cortical forma parte de las conocidas | + | La '''displasia cortical focal''' ('''DCF''') ocurre cuando las células cerebrales (o neuronas) en desarrollo de un [[embrión]] o [[feto]] no logran alcanzar las partes de la materia gris del cerebro para las que están destinadas genéticamente. Como resultado, aquellas áreas de la corteza carecen de las conexiones neuronales apropiadas para funcionar correctamente. Las áreas corticales afectadas pueden ser pequeñas y definidas o pueden incluir a todo un hemisferio del cerebro. |
| + | |||
| + | La displasia cortical forma parte de las conocidas «malformaciones del desarrollo cortical» (MDC), un grupo variado de patologías que destaca principalmente por un desarrollo alterado de la estructura de la corteza cerebral. | ||
== Antecedente == | == Antecedente == | ||
| − | |||
| − | + | La primera descripción de «displasias focales» fue realizada por Taylor en pacientes con epilepsia fármacorresistente, para describir anormalidades focales de la estructura de la corteza cerebral caracterizadas por alteración de laminación, neuronas dismórficas y células en balón.<ref>Harding BN, Copp AJ. «Malformations», en: Graham DI, Lantos PL (eds.): ''Greenfield’s Neuropathology''. 7th Ed. London: Arnold; 2002, Vol I, Chapt 7, p. 357-483. en 1971</ref> | |
| − | + | Los mecanismos fisiopatológicos por cuales las DCF<!--los acrónimos no se pluralizan--> generan epilepsias no son claros.<ref>Lahl, R.; Villagrán, R.; Teixeira, W. (2000): «Neuropatología de las epilepsias sintomáticas con consideración especial de las formas focales crónicas resistentes al tratamiento medicamentoso». En: Cruz, S. F. F. (ed.): ''Neuropatología. Diagnóstico y clínica''. [[Madrid]] (España): EDIMSA; capítulo 37, pág. 828-878; 2000.</ref> | |
| − | + | Sin embargo, el tejido displásico tendría una epileptogenicidad intrínseca.<ref>Kalter H. (1991): «Five-decade international trends in the relation of perinatal mortality and congenital malformations: still-birth and neonatal death compared», artículo en la revista ''International Journal of Epidemiology'', 20: págs. 173-179; 1991.</ref> | |
| − | + | == Desarrollo embriológico de la corteza cerebral == | |
| − | + | [[Archivo:Dcf5.JPG|miniatura|Figura 1. [[Corteza cerebral]]. Nótese el engrosamiento de la sustancia gris cortical y la mala definición entre la sustancia gris y la sustancia blanca.]] | |
| − | + | El [[cerebro]] se comienza a desarrollar antes del nacimiento, en el período intrauterino y pasa por diversas fases que pueden solaparse entre sí. | |
| − | + | La corteza cerebral tiene una estructura altamente organizada y se encuentra ampliamente conectada con el resto de las estructuras encefálicas y la [[médula espinal]]. Su formación es compleja y ocurre en etapas temporal y espacialmente ordenadas, incluso con la formación de estructuras transitorias que finalmente desaparecen. | |
| − | + | Se han identificado tres principales etapas consecutivas del desarrollo de la corteza cerebral, cada una parcialmente sobrepuesta con la siguiente, conocidas como: «etapa de proliferación y diferenciación celular», «etapa de migración neuronal» y «etapa de organización cortical».<ref>Blümcke, I., et al. (2002): «Ammon’s horn sclerosis: a maldevelopmental disorder associated with temporal lobe epilepsy», en ''Brain Pathology'', 12: págs. 199-211; 2002.</ref><ref>Kuzniecky, R. I., et al. (1998): «Temporal lobe developmental malformations andepilepsy. Dual pathology and bilateral hippocampal abnormalities», en ''Neurology'', 1998; 50: págs. 748-754.</ref><ref>Wolf, H. K., et al. (1995): «Glioneuronal malformative lesions and dysembryoplastic neuroepithelial tumors in patients with chronic pharmacoresistant epilepsies», artículo en ''Journal of Neuropathy Experimental Neurology'', 1995; 34: págs. 245-254.</ref> | |
| − | *La | + | * La «etapa de proliferación y diferenciación celular» ocurre a nivel periventricular en el interior de la matriz germinal, entre la 5.<sup>ta</sup> y 20.<sup>ma</sup> semana de [[gestación]]. Las células germinales se multiplican y se diferencian tanto en neuronas como en células guales. |
| + | * La «etapa de migración» ocurre entre la 6.<sup>ta</sup> y 22.<sup>da</sup> semanas de gestación. En esta etapa, las neuronas se adhieren a una fibra glial radial y cambian de posición desde la región periventricular hasta su posición final en la corteza cerebral. | ||
| + | * La corteza cerebral normal contiene numerosas células, localizadas en sitios específicos que le otorgan una arquitectura característica; se organiza en 6 capas que se enumeran desde la capa I, o molecular, hasta la capa VI o capa multiforme, sin embargo el proceso de migración se produce desde las capas más profundas hasta las capas más superficiales. | ||
| + | * La «etapa de organización cortical», que depende en parte del proceso de migración, ocurre entre las 22.<sup>da</sup> semana de gestación hasta los 2 años de vida. Las neuronas se diferencian en distintos subtipos celulares como células piramidales, células estrelladas, células multipolares y otras, que se organizan en láminas horizontales, conformando un patrón [[célula|cito]]arquitectónico cortical normal. | ||
Las etapas principales del desarrollo de la corteza cerebral son la proliferación y diferenciación celular, migración y organización de las células en sus áreas correspondientes y mielinización. | Las etapas principales del desarrollo de la corteza cerebral son la proliferación y diferenciación celular, migración y organización de las células en sus áreas correspondientes y mielinización. | ||
| + | |||
Evidentemente, si hay cualquier tipo de alteración en estos procesos el desarrollo cortical va a verse perjudicado y se reflejará en diversos déficits cognitivos y conductuales. | Evidentemente, si hay cualquier tipo de alteración en estos procesos el desarrollo cortical va a verse perjudicado y se reflejará en diversos déficits cognitivos y conductuales. | ||
| − | + | [[Histología|Histológicamente]] se definen las siguientes capas: | |
| − | *La capa I | + | * La capa I (molecular) no tiene neuronas. |
| − | *La células piramidales se localizan en las capas III | + | * La células piramidales se localizan en las capas III (piramidal externa). |
| − | *La capa V | + | * La capa V (piramidal interna); se caracterizan por su tamaño y orientación perpendicular a la superficie cortical. Las células piramidales normales de mayor tamaño se localizan en la capa V. |
=== Abnormalidad === | === Abnormalidad === | ||
| + | |||
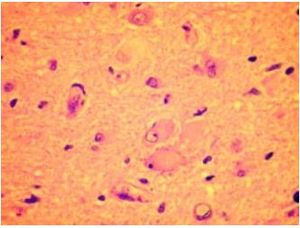
| + | [[Archivo:Dcf6.JPG|miniatura|Figura 2. [[Corteza cerebral]]. DCF. La capa molecular aparece a la derecha de la imagen. La microfotografía muestra grupos de neuronas grandes y pequeñas, irregularmente dispersos en el espesor de las capas corticales. Corte teñido con método inmunohistoquímico para NeuN.]] | ||
| + | |||
Las tres etapas del desarrollo cortical normal no se encuentran temporalmente separadas, la proliferación continúa luego que la migración comienza y la migración continúa después que se ha realizado. Hay que destacar que la célula que resulta de una proliferación anormal, frecuentemente no migra ni se organiza adecuadamente. | Las tres etapas del desarrollo cortical normal no se encuentran temporalmente separadas, la proliferación continúa luego que la migración comienza y la migración continúa después que se ha realizado. Hay que destacar que la célula que resulta de una proliferación anormal, frecuentemente no migra ni se organiza adecuadamente. | ||
| − | + | ''a'') Alteraciones de la proliferación: | |
| − | Las alteraciones de la proliferación se manifiestan por una disminución de la proliferación | + | |
| + | Las alteraciones de la proliferación se manifiestan por una disminución de la proliferación (micro-lisencefalia), por un aumento de la proliferación celular (hemimegalencefalia) o por una proliferación anormal (displasia cortical focal tipo II). | ||
| − | + | ''b'') Alteraciones de migración: | |
| − | |||
| − | + | Las alteraciones de la migración pueden producir una disminución de la migración (lisencefalia), una detención precoz de la migración con neuronas mal posicionadas a nivel periventricular o en la sustancia blanca (heterotopía periventricular o en banda), o en una sobremigración (distrofia muscular congénita). | |
| − | Las alteraciones de la | ||
| − | '''' | + | ''c'') Alteraciones de la organización: |
| + | |||
| + | Las alteraciones de la organización producen trastornos de la estructura de la corteza como la polimicrogiria, esquizencefalia o displasias corticales focales tipo I. | ||
| + | |||
| + | Desde el punto de vista de la imaginología, las alteraciones producidas durante la fase de proliferación se pueden extender desde los ventrículos hasta la superficie pial, mientras que las alteraciones de la fase de migración se localizan en la sustancia blanca y/o corteza. En general, las alteraciones de la organización se encuentran limitadas a la corteza cerebral.<ref>Schwartzkroin, P. A.; y Walsh, C. A. (2000): «Cortical malformations and epilepsy», artículo en la revista ''Mental Retardation and Developmental Disabilities Research Reviews'', 6 (4): págs. 268-280.</ref> | ||
== Epidemiología == | == Epidemiología == | ||
| − | Se estima que un | + | |
| + | Se estima que un 76 % de los pacientes con DCF<!--los acrónimos no se pluralizan--> sufren de epilepsia refractaria,<ref>Yang QH, et al. (1997): «Trends and patterns of mortality associated with birth defects and genetic diseases in the United States 1979-1992: an analysis of multiple-cause mortality data», artículo en la revista ''Genetic Epidemiology'', 14: págs. 493-505; 1997.</ref> mientras que en un 25 % de los pacientes con crisis epilépticas parciales se ha identificado una DCF como la causa subyacente.<ref name=Taylor_Falconer_Burton_Corsellis_1971>Taylor, D. C.; Falconer, M. A.; Burton, C. J.; Corsellis, J. A. (1971): «Focal dysplasia of the cerebral cortex in epilepsy», artículo en ''Journal of Neurology, Neurosurgery, and Psychiatry'', 34: págs. 369-387; 1971.</ref> | ||
== Síntomas == | == Síntomas == | ||
| − | |||
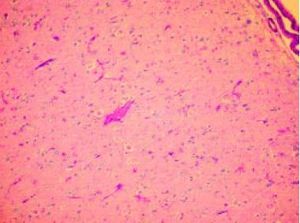
| − | * | + | [[Archivo:Dcf7.JPG|miniatura|Figura 3. [[Corteza cerebral]]. DCF. Se aprecia dislaminación y desorganización neuronal. Nótese las neuronas gigantes, dismórficas en el espesor cortical. Asimismo, hay abundantes neuronas ectópicas en la capa molecular. Tinción con hematoxilina y eosina.]] |
| − | ** | + | |
| + | Las «convulsiones recurrentes» en un infante o en un niño muy pequeño son el [[síntoma]] más común de displasia cortical. La actividad cerebral epiléptica que procede de la displasia cortical aparece de modo muy temprano en la vida de un [[niño]] afectado porque las anomalías de la corteza ocurren desde el [[útero]] y ya están presentes al nacer. Otros síntomas neurológicos variarán dependiendo de cuáles partes del cerebro están afectadas. | ||
| + | |||
| + | * '''Déficits neurológicos focales''': suponen problemas en alguna parte concreta de nuestro funcionamiento debidos a causas cerebrales. | ||
| + | ** Pueden ser muy variados como: la sensibilidad de un lado de la cara, el movimiento de una extremidad, la visión de un [[ojo]], dificultades para expresar el habla, problemas de control emocional, etc. | ||
| − | * | + | * '''Problemas intelectuales''': incluso algunas veces puede asociarse con un nivel de inteligencia por debajo de la media, problemas para concentrarse y dificultades para aprender cosas nuevas. |
| − | * | + | * '''Retraso en el desarrollo cognitivo y psicomotor''': la mejor manera de saber cómo se está desarrollando un niño pequeño es observar su capacidad motora. |
== Características macroscópicas de la DCF == | == Características macroscópicas de la DCF == | ||
| − | |||
| − | Al corte, la | + | En la mayoría de los casos la DCF, como su nombre lo indica, se halla restringida a una o dos circunvoluciones que aparecen ensanchadas y de aspecto anormal (disgiria) en cualquiera de los lóbulos cerebrales, más frecuentemente en el lóbulo temporal. |
| + | |||
| + | Al corte, la sustancia gris puede estar engrosada; la zona de unión con la sustancia blanca muestra límite impreciso, borroso, difícil de establecer con exactitud, a veces puede haber islotes ectópicos de sustancia gris en la blanca. | ||
== Características histológicas == | == Características histológicas == | ||
| − | [[ | + | |
| − | La DCFT se caracteriza por desorganización laminar de variable intensidad, con la consiguiente pérdida de la organización columnar y, en los casos graves, presencia en el espesor cortical de neuronas gigantes, dismórficas, ectópicas, mal orientadas, con citoesqueleto relevante desorganizado, caóticamente dispersas en todas las capas corticales excepto en la primera capa; asimismo hay | + | [[Archivo:Dcf4.JPG|miniatura|Corteza cerebral. DCF. Células globoides («balonadas») en la sustancia blanca subcortical. Tinción con hematoxilina y eosina.]] |
| + | |||
| + | La DCFT se caracteriza por desorganización laminar de variable intensidad, con la consiguiente pérdida de la organización columnar y, en los casos graves, presencia en el espesor cortical de neuronas gigantes, dismórficas, ectópicas, mal orientadas, con citoesqueleto relevante desorganizado, caóticamente dispersas en todas las capas corticales excepto en la primera capa; asimismo hay proliferación glial astrocitaria, con ausencia (DCF tipo II A) o presencia de bizarras células globoides (balonadas) (DCF tipo II B). | ||
=== Otras alteraciones corticales === | === Otras alteraciones corticales === | ||
| − | |||
| − | Recientemente se describe que algunas de las neuronas citomegálicas, comúnmente presentes en la DCF son en realidad interneuronas,<ref>André | + | Se caracterizan por excrecencias de [[tejido]] glioneuronal en las leptomeninges, persistencia de abundantes neuronas en la capa cortical I (molecular) y en la sustancia blanca subcortical abundantes neuronas ectópicas y células globoides (balonadas) que semejan astrocitos gemistocíticos, ya que tienen citoplasma abundante, ovoide, de contenido semitransparente, [[eosinófilo]]. Límites imprecisos entre sustancia gris y sustancia blanca. Hamartomatosis glioneuronal: focos de elementos gliales y neuronales maduros, a veces mezclados con células oligodendroglioides (en 15 % de cerebros con epilepsia). |
| − | in severe pediatric cortical | + | |
| + | Recientemente se describe que algunas de las neuronas citomegálicas, comúnmente presentes en la DCF son en realidad interneuronas,<ref>André, V. M., et al. (2007): «Cytomegalic interneurons: a new abnormal cell type in severe pediatric cortical dysplasia», artículo en ''Journal of Neuropathology and Experimental Neurology'', 66: págs. 491-504; 2007.</ref> lo cual ―además de constituir una reidentificación de esa estructura― tiene significado fisiológico como participante importante en la génesis de las convulsiones, ya que forman parte de circuitos neuronales anormales en la zona afectada.<ref>Crino, P. B.; Miyata, H.; y Vinters, H. V. (2002): «Neurodevelopmental disorders as a cause of seizures: neuropathologic, genetic, and mechanistic considerations», artículo en Brain Pathology'', 12: págs. 212-233; 2002.</ref><ref>Ferrer, I.; Pineda, M., et al.: «Abnormal-local circuit neurons in epilepsia partialis continua associated with focal cortical dysplasia», artículo en la revista ''Acta Neuropathology'', 83: págs. 246-259. Berlín, 1992. Es evidente que las interneuronas citomegálicas en la DCF son hiperexcitables.</ref> | ||
El signo más relevante es el aumento de la frecuencia de descarga en comparación con las interneuronas normales. | El signo más relevante es el aumento de la frecuencia de descarga en comparación con las interneuronas normales. | ||
== Clasificación de la DCF == | == Clasificación de la DCF == | ||
| − | Existen varias clasificaciones, que se aplican indistintamente en la literatura correspondiente. La mayoría de esas clasificaciones se basan en la estructura histológica de las | + | |
| + | Existen varias clasificaciones, que se aplican indistintamente en la literatura correspondiente. La mayoría de esas clasificaciones se basan en la estructura histológica de las malformaciones corticales, en los hallazgos en los estudios de neuroimagen, sobre todo los de resonancia magnética y en la correlación con las manifestaciones clínicas y los aspectos electroencefalográficos.<ref name=Taylor_Falconer_Burton_Corsellis_1971/><ref>Mackay MT, et al. (2003): «Malformations of cortical development with balloon cells: clinical and radiological correlates», artículo en ''Neurology'', 60: págs. 580-587; 2003.</ref><ref>Lawson JA, et al. (2005): «Distinct clinicopathologic subtypes of cortical dysplasia of Taylor», artículo en ''Neurology'', 64: págs. 55-61; 2005.</ref><ref>Tassi I, et al. (2002): «Focal cortical dysplasia: neuropathological subtypes, EEG, neuroimaging and surgical outcome», artículo en revista ''Brain'', 125: págs. 1719-1732; 2002.</ref><ref name=Palmini_2004>Palmini, A., et al. (2004): «Terminology and classification of the cortical dysplasias», artículo publicado en la revista ''Neurology'' 62 (suplemento 3), págs. S1-S8; 2004.</ref><ref>Barkovich AJ, et al. (2001): «Classification system for malformations of cortical development: update 2001», artículo en ''Neurology'', 57: págs. 2168-2178; 2001.</ref><ref>Rickert, C. H. (2015): «Cortical dysplasia: neuropathological aspects», artículo en revista ''Child’s Nervous System'', 22: págs. 821-826; 2006.</ref> | ||
| + | Más recientemente han aparecido clasificaciones que incluyen los aspectos genéticos de cada una de las malformaciones (tabla 1).<ref name=Tassi_I/> | ||
<center>'''Tabla 1. Clasificación de malformaciones corticales en epilepsia*'''</center> | <center>'''Tabla 1. Clasificación de malformaciones corticales en epilepsia*'''</center> | ||
| Línea 110: | Línea 129: | ||
| Esencial para la migracion | | Esencial para la migracion | ||
|- | |- | ||
| − | | | + | | |
| Lisencefalia | | Lisencefalia | ||
| Lis 1 | | Lis 1 | ||
| Línea 118: | Línea 137: | ||
|- | |- | ||
| Migración interrumpida | | Migración interrumpida | ||
| − | | Lisencefalia | + | | Lisencefalia (XLIS) heterotropia laminar |
| − | | DCX (XLIS) | + | | DCX (XLIS). |
| Doblecortin | | Doblecortin | ||
| Liga y estabiliza tubulina en neuronas en migración | | Liga y estabiliza tubulina en neuronas en migración | ||
| Línea 131: | Línea 150: | ||
| Falla de laminación cortical | | Falla de laminación cortical | ||
| Displasia cortical focal | | Displasia cortical focal | ||
| − | | TSC polimorfismo de TSC (y cdk 5) | + | | TSC polimorfismo de TSC (y cdk 5). |
| − | | Hamartina (Cdk 5) | + | | Hamartina (Cdk 5). |
| Interactúa con la ERM, contribuye a la adhesion y tamaño celular | | Interactúa con la ERM, contribuye a la adhesion y tamaño celular | ||
|- | |- | ||
| − | | | + | | |
| Microdisgénesis | | Microdisgénesis | ||
| Presenilina 1 | | Presenilina 1 | ||
| − | | | + | | |
| − | | | + | | |
|- | |- | ||
| Desconocido | | Desconocido | ||
| Línea 147: | Línea 166: | ||
| Gene homeobox que conforma el cerebro | | Gene homeobox que conforma el cerebro | ||
|- | |- | ||
| − | | | + | | |
| Polimicrogiria focal y generalizada | | Polimicrogiria focal y generalizada | ||
| PAX 6 mutación identificada en parientes | | PAX 6 mutación identificada en parientes | ||
| Línea 155: | Línea 174: | ||
=== Clasificación propuesta por Tassi === | === Clasificación propuesta por Tassi === | ||
| − | La clasificación propuesta por Tassi<ref>Tassi I, et al. | + | |
| + | [[Archivo:Dcf8.JPG|miniatura|Figura 4. [[Corteza cerebral]]. DCF. Abundantes neuronas displásicas con neuritas irregulares, y prominente [[citoplasma]], dispersas desordenadamente en las capas corticales. Tinción para neurofilamentos.]] | ||
| + | |||
| + | La clasificación propuesta por Tassi se basa en la neuropatología, más datos de neuroimagen y genética.<ref name=Tassi_I>Tassi, I., et al. (2002): «Focal cortical dysplasia: neuropathological subtypes, EEG, neuroimaging and surgical outcome», artículo en la revista ''Brain'', 125: págs. 1719-1732; 2002.</ref> | ||
| + | Esta clasificación reconoce tres subtipos histológicos: | ||
| + | displasia arquitectónica, | ||
| + | displasia citoarquitectónica y | ||
| + | displasia cortical focal de Taylor, en dos variedades: la DCF sin células globoides pero con neuronas dismórficas; la DCFT con células globoides, que constituyen su característica principal. | ||
=== Clasificación propuesta por Palmini === | === Clasificación propuesta por Palmini === | ||
| − | |||
| − | #'''Malformación leve de desarrollo cortical | + | La clasificación propuesta por Palmini resulta práctica para exponer las características histológicas:<ref name=Palmini_2004/> |
| − | * | + | |
| − | * | + | #'''Malformación leve de desarrollo cortical''': |
| − | #'''DCF | + | * Tipo I: Neuronas ectópicas en la capa I, capa molecular de la neocorteza |
| − | * | + | * Tipo II: Heterotopia neuronal microscópica en capas neocorticales pero no en la capa I, grupos de neuronas mal colocadas. |
| − | * | + | #'''DCF''': |
| − | * | + | * Tipo I A: Laminación irregular |
| − | * | + | * Tipo I B: Neuronas gigantes o inmaduras |
| + | * Tipo II A: Neuronas dismórficas pero no células globoides. | ||
| + | * Tipo II B: Neuronas dismórficas y células globoides | ||
=== Clasificación que propone Barkovich === | === Clasificación que propone Barkovich === | ||
| − | La clasificación que propone | + | |
| − | # Malformaciones debidas a | + | La clasificación que propone Barkovich considera tres grupos: |
| + | # Malformaciones debidas a proliferación/[[apoptosis]] anormal. | ||
# Malformaciones debidas a migración anormal. | # Malformaciones debidas a migración anormal. | ||
# Malformaciones debidas a migración neuronal anormal tardía. | # Malformaciones debidas a migración neuronal anormal tardía. | ||
== Diagnóstico == | == Diagnóstico == | ||
| + | |||
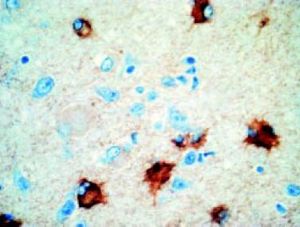
| + | [[Archivo:Dcf9.JPG|miniatura|Figura 5. [[Corteza cerebral]]. DCF. [[Células globoides]] (balonadas) en la sustancia blanca subcortical, positivas para proteína acídica glial fibrilar.]] | ||
| + | |||
La displasia cortical puede ser difícil de diagnosticar porque las partes afectadas del cerebro varían en cada individuo, pero realizan a través de: | La displasia cortical puede ser difícil de diagnosticar porque las partes afectadas del cerebro varían en cada individuo, pero realizan a través de: | ||
* Examen neurológico. | * Examen neurológico. | ||
| − | * | + | * [[Tomografía axial computarizada]] y resonancia magnética. |
* [[Electroencefalograma]]. | * [[Electroencefalograma]]. | ||
==Tratamiento == | ==Tratamiento == | ||
| + | |||
Está centrado en el tratamiento y el control de las convulsiones que resultan de la condición, y los métodos utilizados varían con cada paciente. Los medicamentos anti-convulsiones son exitosos en algunos individuos, mientras que otros pueden tener convulsiones tan severas y difíciles de manejar, que la opción más efectiva puede ser la [[cirugía]] para extraer la porción anormal del [[cerebro]]. | Está centrado en el tratamiento y el control de las convulsiones que resultan de la condición, y los métodos utilizados varían con cada paciente. Los medicamentos anti-convulsiones son exitosos en algunos individuos, mientras que otros pueden tener convulsiones tan severas y difíciles de manejar, que la opción más efectiva puede ser la [[cirugía]] para extraer la porción anormal del [[cerebro]]. | ||
| − | == | + | == Fuentes == |
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | |||
| − | + | {{listaref}} | |
| − | *[https://muyfitness.com/que-es-la-displasia-cortical_13106947/ | + | :* Escobar, Alfonso; Boleaga, Bernardo; Vega Gama, J. Gustavo; Weidenheim, Karen M. (2008): [http://revmexneuroci.com/wp-content/uploads/2014/06/Nm083-10.pdf «Displasia cortical focal y epilepsia»], informe de caso. ''Revista Mexicana de Neurociencia'', 9 (3): págs. 231-238; mayo-junio de 2008. Consultado el 9 de agosto de 2018. |
| − | *[http://www.epilepsiamadrid.com/2016/02/07/el-uso-de-rm-de-7-t-mejora-la-deteccion-de-displasias-corticales-en-un-30/ | + | :* Kerns, Michelle (2017): [https://muyfitness.com/que-es-la-displasia-cortical_13106947/ «¿Qué es la displasia cortical?»], artículo publicado el 18 de julio de 2017 en el sitio web Muy Fitness. |
| − | + | :* Martos Silván, Cinta (2018): [https://www.lifeder.com/displasia-cortical/ «Displasia cortical: causas, síntomas y tratamiento»], artículo publicado en el sitio web Lifeder. Consultado el 9 de agosto de 2018. | |
| − | + | :* [http://www.epilepsiamadrid.com/2016/02/07/el-uso-de-rm-de-7-t-mejora-la-deteccion-de-displasias-corticales-en-un-30/ «El uso de la resonancia magnética de 7T mejora la detección de displasias corticales en un 30 %»], artículo publicado el 7 de febrero de 2016 en el sitio web Epilepsia Madrid (España). Consultado el 9 de agosto de 2018. | |
| − | *[https://scielo.conicyt.cl/scielo.php?script=sci_arttext&pid=S0717-93082009000400005 | + | :* [https://scielo.conicyt.cl/scielo.php?script=sci_arttext&pid=S0717-93082009000400005 «Displasis corticales como causa de epilepsia y sus representaciones en las imágenes»], artículo publicado en la ''Revista Chilena de Radiología'', versión en línea; 15 (suplemento 1): págs. s25-s38; 2009. ISSN 0717-9308. Consultado el 9 de agosto de 2018. |
| − | [[ | + | [[Categoría: Enfermedades]] |
| − | [[ | + | [[Categoría: Neurología]] |
Revisión del 04:11 14 ago 2018
| ||||||||||
La displasia cortical focal (DCF) ocurre cuando las células cerebrales (o neuronas) en desarrollo de un embrión o feto no logran alcanzar las partes de la materia gris del cerebro para las que están destinadas genéticamente. Como resultado, aquellas áreas de la corteza carecen de las conexiones neuronales apropiadas para funcionar correctamente. Las áreas corticales afectadas pueden ser pequeñas y definidas o pueden incluir a todo un hemisferio del cerebro.
La displasia cortical forma parte de las conocidas «malformaciones del desarrollo cortical» (MDC), un grupo variado de patologías que destaca principalmente por un desarrollo alterado de la estructura de la corteza cerebral.
Sumario
Antecedente
La primera descripción de «displasias focales» fue realizada por Taylor en pacientes con epilepsia fármacorresistente, para describir anormalidades focales de la estructura de la corteza cerebral caracterizadas por alteración de laminación, neuronas dismórficas y células en balón.[1]
Los mecanismos fisiopatológicos por cuales las DCF generan epilepsias no son claros.[2] Sin embargo, el tejido displásico tendría una epileptogenicidad intrínseca.[3]
Desarrollo embriológico de la corteza cerebral
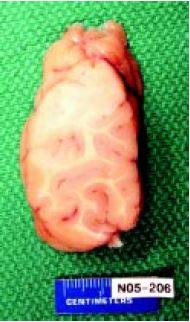
El cerebro se comienza a desarrollar antes del nacimiento, en el período intrauterino y pasa por diversas fases que pueden solaparse entre sí.
La corteza cerebral tiene una estructura altamente organizada y se encuentra ampliamente conectada con el resto de las estructuras encefálicas y la médula espinal. Su formación es compleja y ocurre en etapas temporal y espacialmente ordenadas, incluso con la formación de estructuras transitorias que finalmente desaparecen.
Se han identificado tres principales etapas consecutivas del desarrollo de la corteza cerebral, cada una parcialmente sobrepuesta con la siguiente, conocidas como: «etapa de proliferación y diferenciación celular», «etapa de migración neuronal» y «etapa de organización cortical».[4][5][6]
- La «etapa de proliferación y diferenciación celular» ocurre a nivel periventricular en el interior de la matriz germinal, entre la 5.ta y 20.ma semana de gestación. Las células germinales se multiplican y se diferencian tanto en neuronas como en células guales.
- La «etapa de migración» ocurre entre la 6.ta y 22.da semanas de gestación. En esta etapa, las neuronas se adhieren a una fibra glial radial y cambian de posición desde la región periventricular hasta su posición final en la corteza cerebral.
- La corteza cerebral normal contiene numerosas células, localizadas en sitios específicos que le otorgan una arquitectura característica; se organiza en 6 capas que se enumeran desde la capa I, o molecular, hasta la capa VI o capa multiforme, sin embargo el proceso de migración se produce desde las capas más profundas hasta las capas más superficiales.
- La «etapa de organización cortical», que depende en parte del proceso de migración, ocurre entre las 22.da semana de gestación hasta los 2 años de vida. Las neuronas se diferencian en distintos subtipos celulares como células piramidales, células estrelladas, células multipolares y otras, que se organizan en láminas horizontales, conformando un patrón citoarquitectónico cortical normal.
Las etapas principales del desarrollo de la corteza cerebral son la proliferación y diferenciación celular, migración y organización de las células en sus áreas correspondientes y mielinización.
Evidentemente, si hay cualquier tipo de alteración en estos procesos el desarrollo cortical va a verse perjudicado y se reflejará en diversos déficits cognitivos y conductuales.
Histológicamente se definen las siguientes capas:
- La capa I (molecular) no tiene neuronas.
- La células piramidales se localizan en las capas III (piramidal externa).
- La capa V (piramidal interna); se caracterizan por su tamaño y orientación perpendicular a la superficie cortical. Las células piramidales normales de mayor tamaño se localizan en la capa V.
Abnormalidad
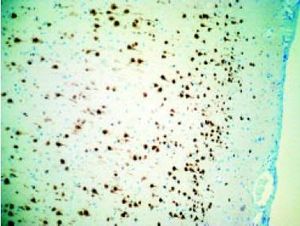
Las tres etapas del desarrollo cortical normal no se encuentran temporalmente separadas, la proliferación continúa luego que la migración comienza y la migración continúa después que se ha realizado. Hay que destacar que la célula que resulta de una proliferación anormal, frecuentemente no migra ni se organiza adecuadamente.
a) Alteraciones de la proliferación:
Las alteraciones de la proliferación se manifiestan por una disminución de la proliferación (micro-lisencefalia), por un aumento de la proliferación celular (hemimegalencefalia) o por una proliferación anormal (displasia cortical focal tipo II).
b) Alteraciones de migración:
Las alteraciones de la migración pueden producir una disminución de la migración (lisencefalia), una detención precoz de la migración con neuronas mal posicionadas a nivel periventricular o en la sustancia blanca (heterotopía periventricular o en banda), o en una sobremigración (distrofia muscular congénita).
c) Alteraciones de la organización:
Las alteraciones de la organización producen trastornos de la estructura de la corteza como la polimicrogiria, esquizencefalia o displasias corticales focales tipo I.
Desde el punto de vista de la imaginología, las alteraciones producidas durante la fase de proliferación se pueden extender desde los ventrículos hasta la superficie pial, mientras que las alteraciones de la fase de migración se localizan en la sustancia blanca y/o corteza. En general, las alteraciones de la organización se encuentran limitadas a la corteza cerebral.[7]
Epidemiología
Se estima que un 76 % de los pacientes con DCF sufren de epilepsia refractaria,[8] mientras que en un 25 % de los pacientes con crisis epilépticas parciales se ha identificado una DCF como la causa subyacente.[9]
Síntomas
Las «convulsiones recurrentes» en un infante o en un niño muy pequeño son el síntoma más común de displasia cortical. La actividad cerebral epiléptica que procede de la displasia cortical aparece de modo muy temprano en la vida de un niño afectado porque las anomalías de la corteza ocurren desde el útero y ya están presentes al nacer. Otros síntomas neurológicos variarán dependiendo de cuáles partes del cerebro están afectadas.
- Déficits neurológicos focales: suponen problemas en alguna parte concreta de nuestro funcionamiento debidos a causas cerebrales.
- Pueden ser muy variados como: la sensibilidad de un lado de la cara, el movimiento de una extremidad, la visión de un ojo, dificultades para expresar el habla, problemas de control emocional, etc.
- Problemas intelectuales: incluso algunas veces puede asociarse con un nivel de inteligencia por debajo de la media, problemas para concentrarse y dificultades para aprender cosas nuevas.
- Retraso en el desarrollo cognitivo y psicomotor: la mejor manera de saber cómo se está desarrollando un niño pequeño es observar su capacidad motora.
Características macroscópicas de la DCF
En la mayoría de los casos la DCF, como su nombre lo indica, se halla restringida a una o dos circunvoluciones que aparecen ensanchadas y de aspecto anormal (disgiria) en cualquiera de los lóbulos cerebrales, más frecuentemente en el lóbulo temporal.
Al corte, la sustancia gris puede estar engrosada; la zona de unión con la sustancia blanca muestra límite impreciso, borroso, difícil de establecer con exactitud, a veces puede haber islotes ectópicos de sustancia gris en la blanca.
Características histológicas
La DCFT se caracteriza por desorganización laminar de variable intensidad, con la consiguiente pérdida de la organización columnar y, en los casos graves, presencia en el espesor cortical de neuronas gigantes, dismórficas, ectópicas, mal orientadas, con citoesqueleto relevante desorganizado, caóticamente dispersas en todas las capas corticales excepto en la primera capa; asimismo hay proliferación glial astrocitaria, con ausencia (DCF tipo II A) o presencia de bizarras células globoides (balonadas) (DCF tipo II B).
Otras alteraciones corticales
Se caracterizan por excrecencias de tejido glioneuronal en las leptomeninges, persistencia de abundantes neuronas en la capa cortical I (molecular) y en la sustancia blanca subcortical abundantes neuronas ectópicas y células globoides (balonadas) que semejan astrocitos gemistocíticos, ya que tienen citoplasma abundante, ovoide, de contenido semitransparente, eosinófilo. Límites imprecisos entre sustancia gris y sustancia blanca. Hamartomatosis glioneuronal: focos de elementos gliales y neuronales maduros, a veces mezclados con células oligodendroglioides (en 15 % de cerebros con epilepsia).
Recientemente se describe que algunas de las neuronas citomegálicas, comúnmente presentes en la DCF son en realidad interneuronas,[10] lo cual ―además de constituir una reidentificación de esa estructura― tiene significado fisiológico como participante importante en la génesis de las convulsiones, ya que forman parte de circuitos neuronales anormales en la zona afectada.[11][12]
El signo más relevante es el aumento de la frecuencia de descarga en comparación con las interneuronas normales.
Clasificación de la DCF
Existen varias clasificaciones, que se aplican indistintamente en la literatura correspondiente. La mayoría de esas clasificaciones se basan en la estructura histológica de las malformaciones corticales, en los hallazgos en los estudios de neuroimagen, sobre todo los de resonancia magnética y en la correlación con las manifestaciones clínicas y los aspectos electroencefalográficos.[9][13][14][15][16][17][18] Más recientemente han aparecido clasificaciones que incluyen los aspectos genéticos de cada una de las malformaciones (tabla 1).[19]
| Mecanismo Defectuoso | Tipo de malformación | GENES | Proteínas | Funcion normal de la proteína |
|---|---|---|---|---|
| Migración Neuronal | Hipertrofia nodular periventricular | FLN 1 | Filamna 1 | Esencial para la migracion |
| Lisencefalia | Lis 1 | Factor activador de plaquetas | Liga con NusEL y tubulina | |
| Migración interrumpida | Lisencefalia (XLIS) heterotropia laminar | DCX (XLIS). | Doblecortin | Liga y estabiliza tubulina en neuronas en migración |
| Lisencefalia e hipoplasia cerebelosa | RLN | Reelina | Señal que detiene neuronas en migración | |
| Falla de laminación cortical | Displasia cortical focal | TSC polimorfismo de TSC (y cdk 5). | Hamartina (Cdk 5). | Interactúa con la ERM, contribuye a la adhesion y tamaño celular |
| Microdisgénesis | Presenilina 1 | |||
| Desconocido | Esquizencefalia | EMX 2 | Emx 2 | Gene homeobox que conforma el cerebro |
| Polimicrogiria focal y generalizada | PAX 6 mutación identificada en parientes | PAX 6 factor de transcripción | Participa en diferenciación y migración neuronal |
Clasificación propuesta por Tassi
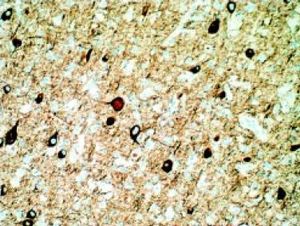
La clasificación propuesta por Tassi se basa en la neuropatología, más datos de neuroimagen y genética.[19] Esta clasificación reconoce tres subtipos histológicos: displasia arquitectónica, displasia citoarquitectónica y displasia cortical focal de Taylor, en dos variedades: la DCF sin células globoides pero con neuronas dismórficas; la DCFT con células globoides, que constituyen su característica principal.
Clasificación propuesta por Palmini
La clasificación propuesta por Palmini resulta práctica para exponer las características histológicas:[16]
- Malformación leve de desarrollo cortical:
- Tipo I: Neuronas ectópicas en la capa I, capa molecular de la neocorteza
- Tipo II: Heterotopia neuronal microscópica en capas neocorticales pero no en la capa I, grupos de neuronas mal colocadas.
- DCF:
- Tipo I A: Laminación irregular
- Tipo I B: Neuronas gigantes o inmaduras
- Tipo II A: Neuronas dismórficas pero no células globoides.
- Tipo II B: Neuronas dismórficas y células globoides
Clasificación que propone Barkovich
La clasificación que propone Barkovich considera tres grupos:
- Malformaciones debidas a proliferación/apoptosis anormal.
- Malformaciones debidas a migración anormal.
- Malformaciones debidas a migración neuronal anormal tardía.
Diagnóstico
La displasia cortical puede ser difícil de diagnosticar porque las partes afectadas del cerebro varían en cada individuo, pero realizan a través de:
- Examen neurológico.
- Tomografía axial computarizada y resonancia magnética.
- Electroencefalograma.
Tratamiento
Está centrado en el tratamiento y el control de las convulsiones que resultan de la condición, y los métodos utilizados varían con cada paciente. Los medicamentos anti-convulsiones son exitosos en algunos individuos, mientras que otros pueden tener convulsiones tan severas y difíciles de manejar, que la opción más efectiva puede ser la cirugía para extraer la porción anormal del cerebro.
Fuentes
- ↑ Harding BN, Copp AJ. «Malformations», en: Graham DI, Lantos PL (eds.): Greenfield’s Neuropathology. 7th Ed. London: Arnold; 2002, Vol I, Chapt 7, p. 357-483. en 1971
- ↑ Lahl, R.; Villagrán, R.; Teixeira, W. (2000): «Neuropatología de las epilepsias sintomáticas con consideración especial de las formas focales crónicas resistentes al tratamiento medicamentoso». En: Cruz, S. F. F. (ed.): Neuropatología. Diagnóstico y clínica. Madrid (España): EDIMSA; capítulo 37, pág. 828-878; 2000.
- ↑ Kalter H. (1991): «Five-decade international trends in the relation of perinatal mortality and congenital malformations: still-birth and neonatal death compared», artículo en la revista International Journal of Epidemiology, 20: págs. 173-179; 1991.
- ↑ Blümcke, I., et al. (2002): «Ammon’s horn sclerosis: a maldevelopmental disorder associated with temporal lobe epilepsy», en Brain Pathology, 12: págs. 199-211; 2002.
- ↑ Kuzniecky, R. I., et al. (1998): «Temporal lobe developmental malformations andepilepsy. Dual pathology and bilateral hippocampal abnormalities», en Neurology, 1998; 50: págs. 748-754.
- ↑ Wolf, H. K., et al. (1995): «Glioneuronal malformative lesions and dysembryoplastic neuroepithelial tumors in patients with chronic pharmacoresistant epilepsies», artículo en Journal of Neuropathy Experimental Neurology, 1995; 34: págs. 245-254.
- ↑ Schwartzkroin, P. A.; y Walsh, C. A. (2000): «Cortical malformations and epilepsy», artículo en la revista Mental Retardation and Developmental Disabilities Research Reviews, 6 (4): págs. 268-280.
- ↑ Yang QH, et al. (1997): «Trends and patterns of mortality associated with birth defects and genetic diseases in the United States 1979-1992: an analysis of multiple-cause mortality data», artículo en la revista Genetic Epidemiology, 14: págs. 493-505; 1997.
- ↑ 9,0 9,1 Taylor, D. C.; Falconer, M. A.; Burton, C. J.; Corsellis, J. A. (1971): «Focal dysplasia of the cerebral cortex in epilepsy», artículo en Journal of Neurology, Neurosurgery, and Psychiatry, 34: págs. 369-387; 1971.
- ↑ André, V. M., et al. (2007): «Cytomegalic interneurons: a new abnormal cell type in severe pediatric cortical dysplasia», artículo en Journal of Neuropathology and Experimental Neurology, 66: págs. 491-504; 2007.
- ↑ Crino, P. B.; Miyata, H.; y Vinters, H. V. (2002): «Neurodevelopmental disorders as a cause of seizures: neuropathologic, genetic, and mechanistic considerations», artículo en Brain Pathology, 12: págs. 212-233; 2002.
- ↑ Ferrer, I.; Pineda, M., et al.: «Abnormal-local circuit neurons in epilepsia partialis continua associated with focal cortical dysplasia», artículo en la revista Acta Neuropathology, 83: págs. 246-259. Berlín, 1992. Es evidente que las interneuronas citomegálicas en la DCF son hiperexcitables.
- ↑ Mackay MT, et al. (2003): «Malformations of cortical development with balloon cells: clinical and radiological correlates», artículo en Neurology, 60: págs. 580-587; 2003.
- ↑ Lawson JA, et al. (2005): «Distinct clinicopathologic subtypes of cortical dysplasia of Taylor», artículo en Neurology, 64: págs. 55-61; 2005.
- ↑ Tassi I, et al. (2002): «Focal cortical dysplasia: neuropathological subtypes, EEG, neuroimaging and surgical outcome», artículo en revista Brain, 125: págs. 1719-1732; 2002.
- ↑ 16,0 16,1 Palmini, A., et al. (2004): «Terminology and classification of the cortical dysplasias», artículo publicado en la revista Neurology 62 (suplemento 3), págs. S1-S8; 2004.
- ↑ Barkovich AJ, et al. (2001): «Classification system for malformations of cortical development: update 2001», artículo en Neurology, 57: págs. 2168-2178; 2001.
- ↑ Rickert, C. H. (2015): «Cortical dysplasia: neuropathological aspects», artículo en revista Child’s Nervous System, 22: págs. 821-826; 2006.
- ↑ 19,0 19,1 Tassi, I., et al. (2002): «Focal cortical dysplasia: neuropathological subtypes, EEG, neuroimaging and surgical outcome», artículo en la revista Brain, 125: págs. 1719-1732; 2002.
- Escobar, Alfonso; Boleaga, Bernardo; Vega Gama, J. Gustavo; Weidenheim, Karen M. (2008): «Displasia cortical focal y epilepsia», informe de caso. Revista Mexicana de Neurociencia, 9 (3): págs. 231-238; mayo-junio de 2008. Consultado el 9 de agosto de 2018.
- Kerns, Michelle (2017): «¿Qué es la displasia cortical?», artículo publicado el 18 de julio de 2017 en el sitio web Muy Fitness.
- Martos Silván, Cinta (2018): «Displasia cortical: causas, síntomas y tratamiento», artículo publicado en el sitio web Lifeder. Consultado el 9 de agosto de 2018.
- «El uso de la resonancia magnética de 7T mejora la detección de displasias corticales en un 30 %», artículo publicado el 7 de febrero de 2016 en el sitio web Epilepsia Madrid (España). Consultado el 9 de agosto de 2018.
- «Displasis corticales como causa de epilepsia y sus representaciones en las imágenes», artículo publicado en la Revista Chilena de Radiología, versión en línea; 15 (suplemento 1): págs. s25-s38; 2009. ISSN 0717-9308. Consultado el 9 de agosto de 2018.